
英文标题:AI-driven prediction of cardio-oncology biomarkers through protein corona analysis
中文标题:通过蛋白冠分析实现心脏肿瘤生物标志物的人工智能驱动预测
发表期刊:Chemical Engineering Journal
影响因子:13.2
研究背景
在心脏肿瘤学领域,前列腺癌(PC)作为美国男性最常见的恶性肿瘤,其转移性(mPC)会导致患者五年生存率从局限性疾病的99%骤降至不足60%,严重威胁患者生命。同时,动脉粥样硬化性心血管疾病(ASCVD)与PC的进展存在密切关联,可通过多种循环因子加剧肿瘤侵袭性和转移扩散,但二者相互作用的具体机制尚未明确。
传统诊断手段如前列腺特异性抗原(PSA)筛查缺乏特异性,而血浆蛋白组学虽为生物标志物发现的首选方法,却受限于血浆蛋白质组的高复杂性和宽动态范围,难以检测低丰度关键蛋白,导致高风险患者的早期诊断和干预滞后。
蛋白质冠作为纳米颗粒表面形成的蛋白质层,能富集传统血浆分析中难以捕捉的低丰度蛋白,显著降低样本复杂性,且其组成可反映健康与疾病状态下的血浆特征,为解决上述挑战提供了新思路。基于此,本研究整合蛋白质冠分析、质谱技术、机器学习与因果推理,旨在揭示ASCVD与mPC的潜在关联生物标志物及机制。
技术路线
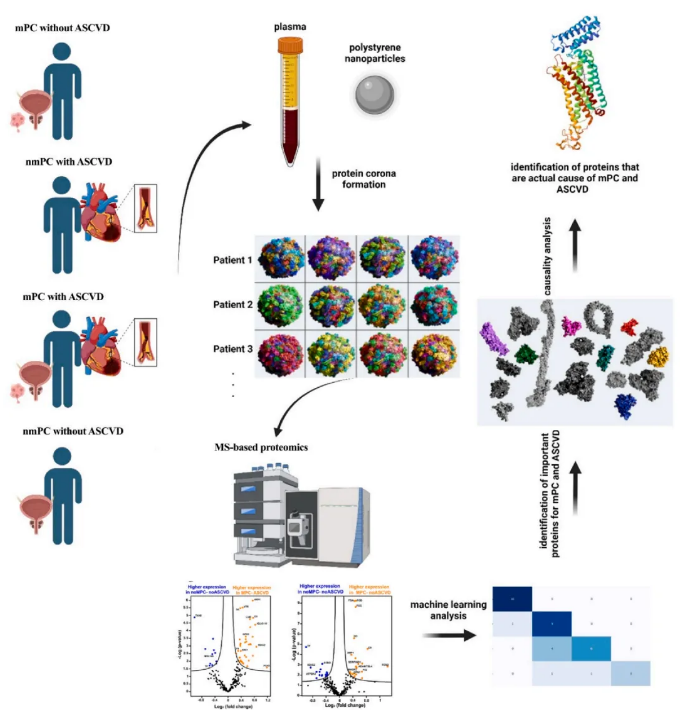
图1. 纳米医学平台示意图
研究结果
1、研究方法与策略
本研究的血浆样本来源于2024年4月就诊于奥古斯塔大学癌症中心的前列腺癌(PC)患者,图1所呈现的纳米医学平台清晰展现了整体检测流程,该平台整合了蛋白冠分析、机器学习算法及实际因果关系评估等关键环节。研究将受试者划分为四组:(1)mPC合并ASCVD组,即患有转移性前列腺癌同时伴有动脉粥样硬化性心血管疾病;(2)ASCVD合并nmPC组,指患有心血管疾病且同时存在非转移性前列腺癌;(3)单纯mPC组,为仅患有转移性前列腺癌而无心血管疾病;(4)nmPC不合并ASCVD组,为非转移性前列腺癌且不合并动脉粥样硬化性心血管疾病。
各组收集的血浆样本与聚苯乙烯纳米颗粒共同孵育后,纳米颗粒表面会形成蛋白冠,随后通过质谱分析和机器学习,筛选出与mPC和ASCVD相关的重要蛋白标志物。
基于质谱的自下而上蛋白质组学(BUP)工作流程可参考图2,该研究共收集了35名PC患者的血浆样本,并按上述方式完成分组。结果显示,57.1%的人群患有高脂血症,且这一情况与亚组分布存在显著相关性。
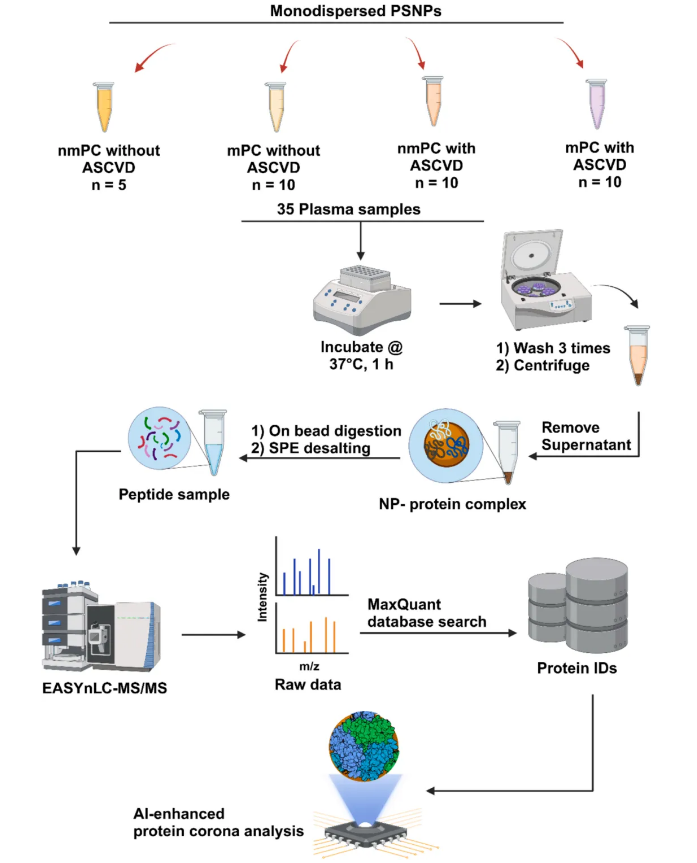
图2. 基于质谱的自下而上蛋白质组学(BUP)工作流程示意图
2、蛋白冠分析
动态光散射(DLS)与zeta电位测定结果显示,相较于原始纳米颗粒(NPs),经处理后的纳米颗粒在粒径和表面电荷上均显著增加(图3A-B),这一变化明确证实了蛋白冠的成功形成。透射电镜(TEM)分析进一步直观呈现了纳米颗粒表面包裹的蛋白冠层(图3A)。
基于质谱的自下而上蛋白质组学(BUP)分析对四组患者的血浆样本进行了蛋白冠组分解析,每组样本均设置三重重复实验,以确保数据的可靠性与重现性(图3C-D)。通过该分析,共鉴定出887种独特蛋白质,其中260种蛋白质在所有样本中稳定检出。
火山图分析(图3C)揭示了这260种共有蛋白质在不同患者组间的表达差异。结合基因本体论(GO)分析(图3D)对这些蛋白质进行深入分类后,发现了关键通路的富集趋势:与单纯mPC患者相比,mPC合并ASCVD患者的蛋白冠中,补体激活、纤维蛋白溶解、血液凝固、先天免疫应答及Arp2/3复合体介导的肌动蛋白成核通路显著富集;此外,GABA能突触、肌母细胞增殖、G蛋白偶联乙酰胆碱受体信号传导、通用信号转导及Rap1信号通路也呈现特异性上调。
通过对四组样本蛋白冠的血浆蛋白质组特征分析(图3),研究揭示这些通路可通过促进慢性炎症、细胞增殖、血管重构及细胞运动性,共同为动脉粥样硬化中的斑块形成与不稳定、癌症中的肿瘤生长、存活及转移创造有利条件。
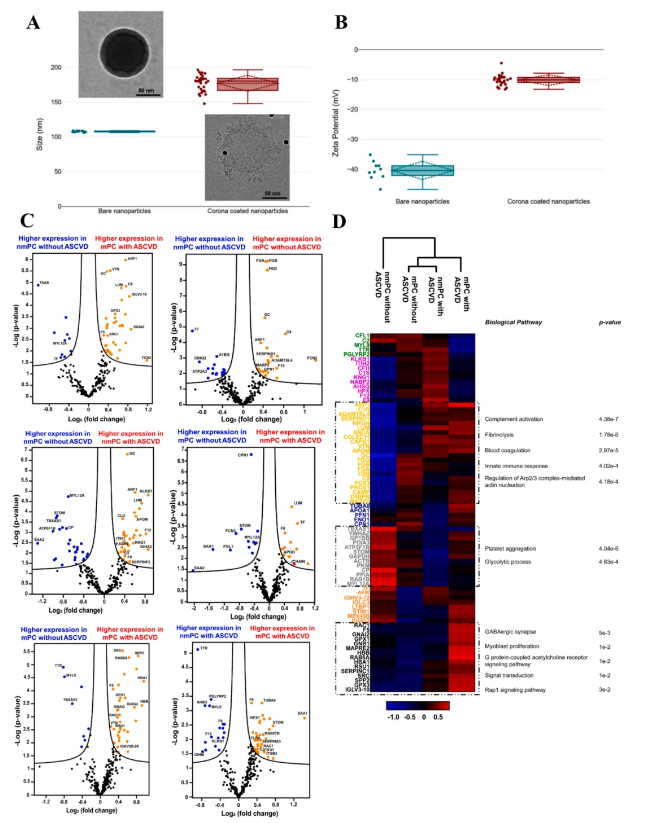
图3. 蛋白冠表征及蛋白质组学分析总结
3、AI-机器学习
基于上述蛋白质组学数据,研究应用AI机器学习方法筛选可稳定区分mPC与ASCVD分组的核心蛋白,采用LASSO正则化(L1正则化)构建逻辑回归模型处理高维度蛋白特征数据。通过网格搜索确定最优正则化系数,在保持验证集分类准确率≥80%的同时最小化非零系数数量,以此降低过拟合风险并精准锁定与mPC/ASCVD分类目标最相关的蛋白子集。
图4A(四组分类混淆矩阵)显示了选定蛋白的分类性能,各组差异蛋白包括:①mPC合并ASCVD组:肌球蛋白轻链3、凝血因子V、甲状腺素运载蛋白、CCT7、肌球蛋白调节轻链多肽9、真核翻译起始因子5A-1、TBXAS1;②ASCVD合并nmPC组:Stomatin蛋白;③单纯mPC组:PRKG1;④单纯nmPC组:淋巴细胞抗原6复合体G6f蛋白、CCT7、Ras相关蛋白Rab-1A等。结合图4B(ASCVD分类混淆矩阵)和图4C(转移分类混淆矩阵)对蛋白与疾病及共病状态的关联分析,共鉴定出22种独特蛋白质,其中ASCVD关联蛋白12种(含CCT7、TBXAS1等),mPC转移关联蛋白11种(含CCT7等)。CCT7是22种蛋白中唯一的共病标志物,凸显其作为心脏肿瘤学双重生物标志物的潜力。
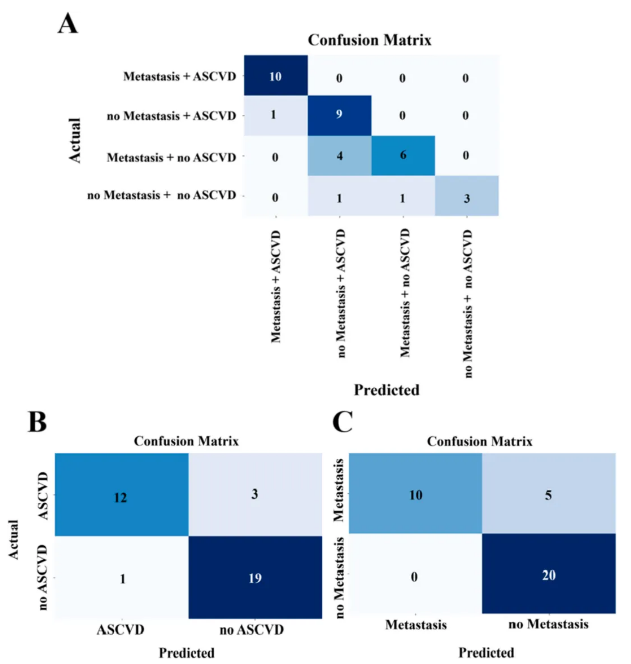
图4. 蛋白质组学分类模型混淆矩阵结果
4、因果关系分析
在因果分析中,该研究初步筛查了全部887种鉴定蛋白,但因样本量有限(仅35例),算法识别出400种潜在因果蛋白。鉴于实际因果蛋白常呈现相关性,该研究转而聚焦机器学习筛选出的22种与ASCVD或mPC显著关联的蛋白。通过精炼因果分析,最终确定血栓素-A合酶1(TBXAS1)、肌动蛋白β及真核翻译起始因子5A-1为ASCVD的实际诱因,其中TBXAS1同时被确定为mPC的因果蛋白。
机器学习筛选出疾病特异性蛋白标志物:肌球蛋白轻链3、凝血因子V、真核翻译起始因子5A-1在mPC合并ASCVD患者中富集,提示其在肌肉收缩、凝血及免疫调节交叉通路中的作用;因果蛋白TBXAS1(仅在蛋白冠中可检测,标准血浆proteomics中未检出)通过促进血小板聚集、血管平滑肌细胞增殖等过程,连接血栓形成与肿瘤进展;而stomatin(ASCVD特异性)与PRKG1(mPC特异性)则体现了生物标志物的疾病背景依赖性。尤为关键的是,22种标志物中唯一同时与ASCVD和mPC相关的蛋白——伴侣蛋白含TCP1亚基7(CCT7),在前列腺腺癌细胞中的表达显著高于早期前列腺肿瘤细胞(DepMap数据库,图5A),其通过调控肿瘤相关蛋白折叠,成为心脏肿瘤学中兼具诊断与治疗价值的新型靶点。图5B进一步验证了TBXAS1的功能相关性,显示其在转移性前列腺腺癌中高表达,为预防癌症转移提供了潜在靶点。
研究揭示,CCT7通过调控炎症反应和血管平滑肌细胞增殖驱动ASCVD进展,其双重关联特性为同时监测心血管疾病与癌症提供了整合视角;因果分析确证的TBXAS1则通过蛋白冠技术被成功捕获,其在血小板聚集和肿瘤-血管相互作用中的关键角色,使其成为ASCVD与mPC的共同治疗靶标。
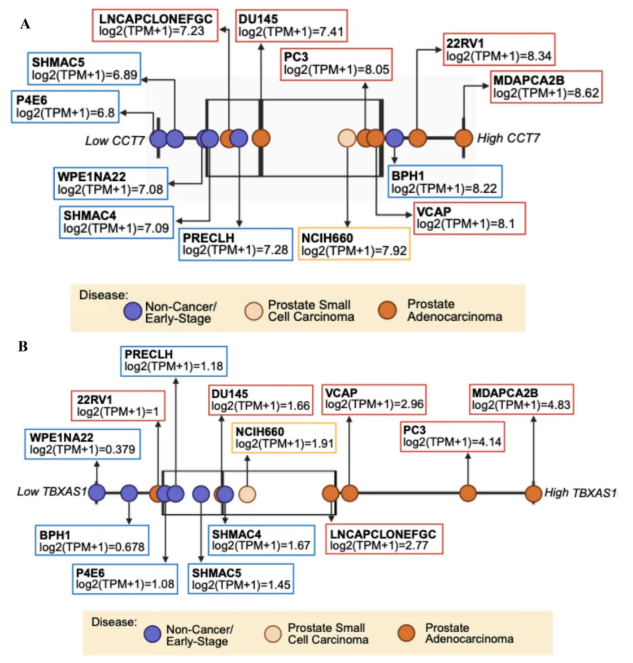
图5. 与早期前列腺癌相比,在转移性前列腺癌和前列腺小细胞癌来源的细胞中CCT7(A)和TBXAS1(B)表达水平更高
研究结论
该研究通过蛋白质组学分析结合AI机器学习方法,筛选出可稳定区分转移性前列腺癌(mPC)与动脉粥样硬化性心血管疾病(ASCVD)及其共病状态的22种显著关联蛋白。因果分析进一步确定TBXAS1等为关键致病因子,其中TBXAS1同时参与两种疾病的病理过程,而CCT7作为唯一双病共有关联蛋白,在转移性前列腺腺癌细胞中高表达,通过调控肿瘤蛋白折叠及炎症反应等机制,成为心脏肿瘤学领域潜在的新型诊断标志物与治疗靶点。研究不仅揭示了mPC与ASCVD共病的分子关联机制,更为两病的精准诊疗提供了重要的蛋白标志物与靶标群。
百趣生物血液蛋白冠-DIA 1X,以纳米材料表面修饰技术为核心支撑,通过纳米颗粒与血清 / 血浆样本的特异性共孵育反应,依托分子间特异性亲和力实现低丰度蛋白的高效富集,进而形成蛋白冠结构。该技术整合样本前处理自动化平台,耦合高灵敏度Astral质谱系统,采用数据非依赖采集(DIA)模式,可实现血液样本的深度蛋白质组学全景分析。相较于常规血液蛋白质组学检测方案,该技术的核心优势在于搭载自主研发的专利磁珠D1(已获国家专利认证)。从磁珠的精密制备到标准化应用流程,均由专业设备与技术团队全程质控,确保磁珠批次间稳定性与均一性。基于此,检测数据呈现出卓越的质量特征:蛋白鉴定数量稳定突破5000+,蛋白稳定检出率达80%以上,同时显著提升功能性指标的检出丰度,为血液蛋白质组学研究提供了高维度、高可靠性的技术解决方案。
若您“血液蛋白冠-DIA 1X”服务感兴趣,百趣生物可提供专业技术服务,欢迎后台私信咨询!