文章标题:Microbiota-derived urocanic acid triggered by tyrosine kinase inhibitors potentiates cancer immunotherapy efficacy
发表期刊:Cell Host & Microbe
影响因子:18.7
客户单位:中国药科大学
百趣提供服务:新一代代谢组学NGM 2 Pro
研究背景
近年来,以抗PD-1/PD-L1抗体为代表的免疫检查点抑制剂(ICB)为多种癌症治疗带来革命性突破,但仅约10%~30%的患者可获得持久响应,多数患者存在原发或继发耐药。酪氨酸激酶抑制剂(TKIs)与ICB联用可显著提升抗肿瘤疗效,但其调控免疫响应的核心机制尚不明确。已有研究表明,TKIs可改变肠道菌群组成,进而间接调节肿瘤免疫微环境。本研究系统揭TKIs诱导肠道菌群中Muribaculum gordoncarteri富集并产生代谢产物尿刊酸(UCA);UCA通过共价结合IκBα的Asp31位点、抑制NF-κB核转位与通路活化,降低趋化因子CXCL1表达,进而减少髓源抑制性细胞(MDSCs)向肿瘤浸润,最终增强抗PD-1免疫治疗的疗效。
研究结果
01.TKls重塑肠道代谢物,打造“抗癌”免疫微环境
为了探究TKls是否通过肠道菌群发挥作用,研究团队设计了一系列精巧的实验。首先收集了接受TKls治疗的结直肠癌患者粪便,从中提取肠道菌群代谢物,并将其给予结直肠癌模型小鼠。
结果显示:与对照组相比,接受TKI诱导的菌群代谢物处理的小鼠,肿瘤数量与体积均显著减少(图1B–E)。对肿瘤微环境的分析进一步发现,抗肿瘤核心效应细胞CD8+ T细胞(尤其是分泌IFN-γ和颗粒酶B的活化杀伤性T细胞)显著增加,而免疫抑制的MDSCs明显减少(图1H–J)。
为确认上述效应依赖肠道菌群,研究人员使用抗生素清除小鼠肠道菌群,结果菌群代谢物的抗肿瘤作用显著减弱。进一步粪菌移植实验证实,只有移植TKls处理小鼠菌群的受体小鼠,肿瘤生长才被显著抑制且生存期延长(图1L–M)。
上述证据链明确表明:TKls可通过重塑肠道菌群及其代谢物,将肿瘤免疫微环境从 “冷肿瘤” 转变为 “热肿瘤”。
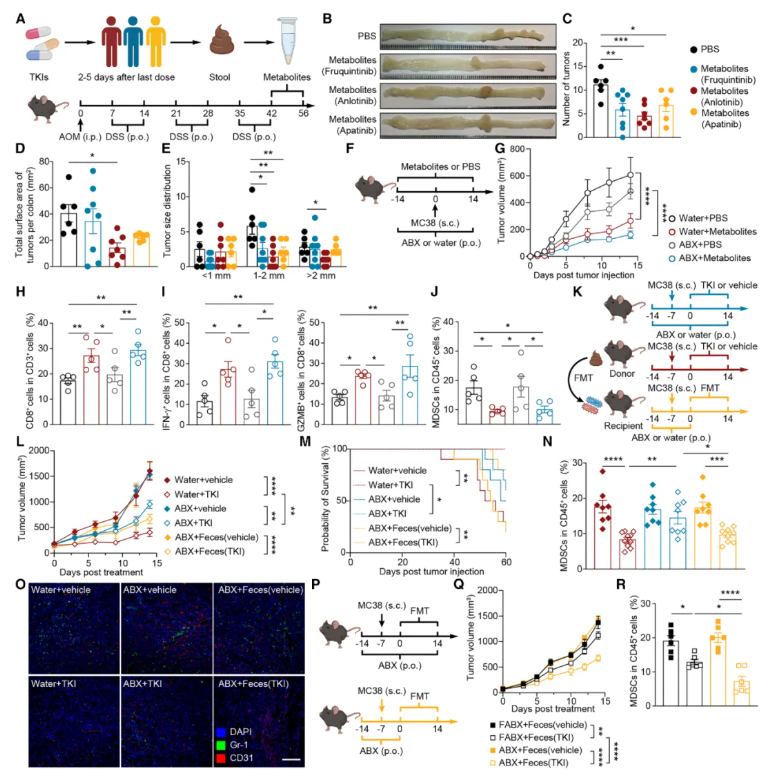
图1.TKIs诱导的肠道微生物代谢物重塑肿瘤微环境
02.锁定关键分子:尿刊酸(UCA)登场
究竟是哪种代谢物在发挥核心作用?团队对小鼠的肠道内容物和血浆进行了全面的代谢组学筛查。结果显示,在TKls处理后,一种名为尿刊酸(Urocanic Acid, UCA)的代谢物水平在小鼠和患者的粪便与血清中均显著升高(图2A–C、2G)。
为了验证UCA的功能,研究人员直接给患癌小鼠补充UCA。结果显示,UCA单独使用即可显著抑制肿瘤生长、延长小鼠生存期,并可减少MDSCs浸润、增强CD8+ T细胞活性(图2I–N)。更重要的是,UCA的抗肿瘤效应不依赖肠道菌群,且体外实验证实UCA不能直接杀伤肿瘤细胞或直接调控免疫细胞功能。这一关键发现表明,UCA并非直接作用于肿瘤或免疫细胞,而是通过调控肿瘤微环境中的细胞招募环节,阻止免疫抑制性的MDSCs进入肿瘤。后续MDSC清除实验进一步证实:当用抗体清除MDSCs后,UCA的抗肿瘤作用完全消失(图2Q–T)。
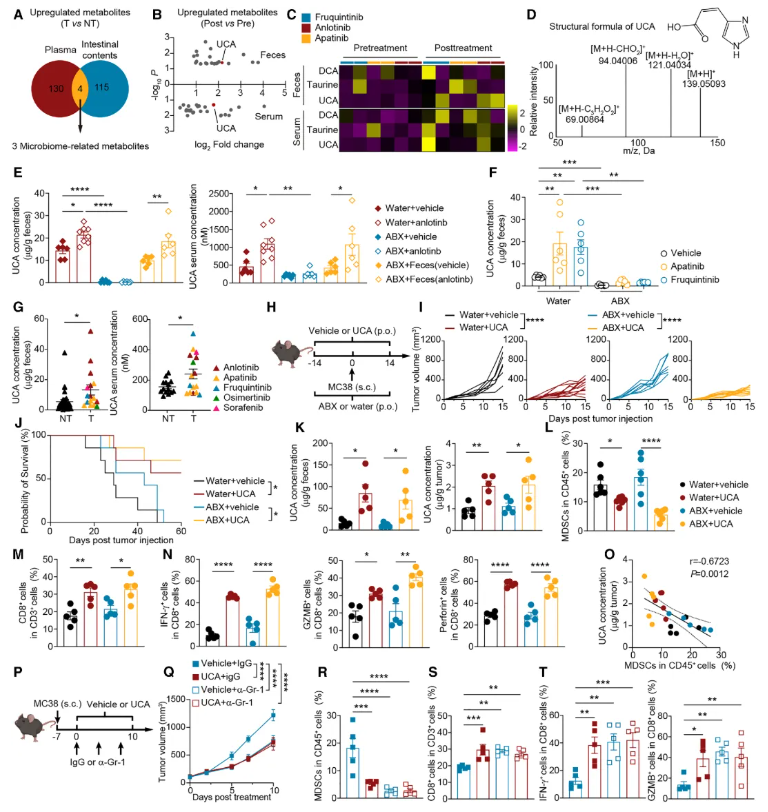
图2.关键代谢物UCA介导MDSC募集抑制
03.追根溯源:揭秘产UCA的“功臣菌”——Muribaculum
UCA水平显著升高,那么产生UCA的核心菌株究竟是什么?通过16S rRNA与宏基因组测序,团队发现TKls处理可显著富集Muribaculum菌属(图3E–F)。该菌属于Muribaculaceae家族,在TKls处理后的患者与小鼠肠道中,其丰度与UCA水平呈显著正相关(图3H)。
为证实Muribaculum是产生UCA的关键菌株,研究人员用Muribaculum gordoncarteri标准菌株并对小鼠进行灌胃。结果显示,补充该菌株后,小鼠肠道UCA水平上升、肿瘤生长受抑、MDSCs浸润减少、CD8+ T细胞活化增强(图3J–M)。为开展终极验证,团队利用基因工程技术,将Muribaculum中合成UCA的关键酶基因hutH+转入大肠杆菌,构建出可直接产生UCA的工程菌株。该工程菌灌胃小鼠后,同样表现出显著的抗肿瘤效果(图3O–R)。反之,若使用能够降解UCA的hutU+工程菌,则会完全逆转上述抗肿瘤与免疫调控效应。这一系列从 “菌群筛选” 到 “菌株验证” 再到 “基因验证” 的完整实验,清晰揭示了TKIs→Muribaculum→UCA的核心调控轴线。
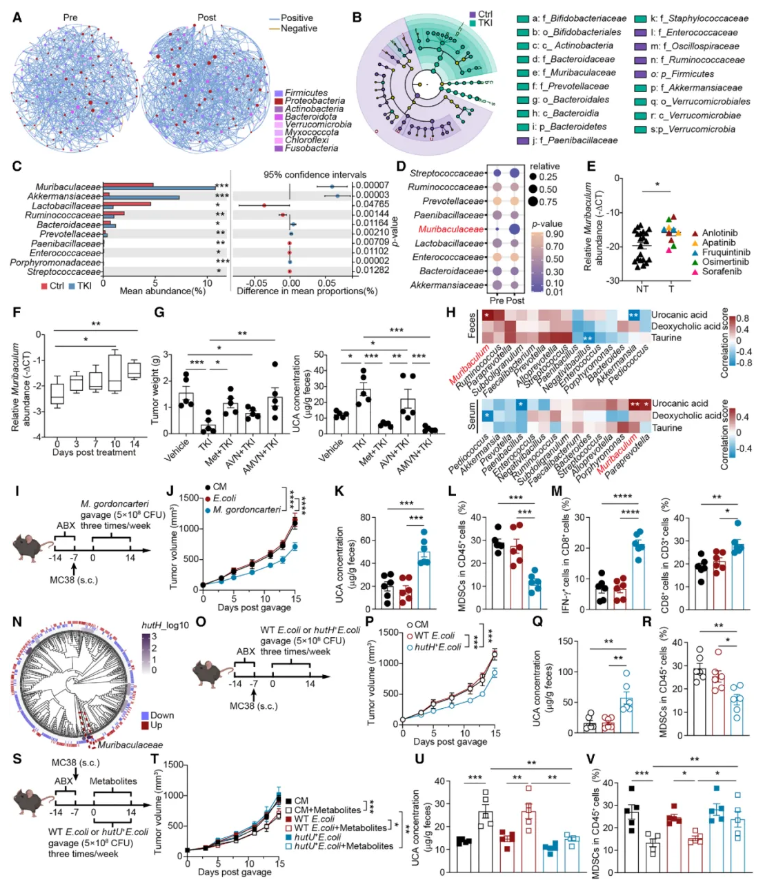
图3.Muribaculum是UCA的主要来源菌属
04.机制揭秘:UCA抑制内皮细胞CXCL1表达以阻断MDSC肿瘤浸润
UCA既然不直接作用于免疫细胞,那它是如何阻止MDSC进入肿瘤的呢?团队利用单细胞测序技术,对UCA处理后的肿瘤微环境进行了高精度解析。结果发现,UCA处理主要影响了肿瘤血管内皮细胞(TECs)(图4I)。内皮细胞是血管的 “守门人”,负责免疫细胞的进出。进一步分析发现,UCA显著抑制了内皮细胞中趋化因子CXCL1的表达(图4I, 5C)。
CXCL1就像一张 “入场券”,专门负责招募表达其受体CXCR2的MDSC进入肿瘤。UCA处理后的肿瘤内皮细胞CXCL1分泌减少,导致MDSC无法被有效募集到肿瘤内部(图5D)。当研究人员用抗体阻断CXCL1或用抑制剂阻断其受体CXCR2后,同样能模拟出类似UCA的抗肿瘤效果(图5O, 5T)。
那么,UCA是如何抑制CXCL1表达的呢?通过分析细胞内信号通路,团队锁定了经典的炎症相关通路——NF-κB通路。UCA处理后,内皮细胞中NF-κB的活化被显著抑制,导致其无法启动下游CXCL1的基因转录(图5I-K)。至此,完整的信号轴浮出水面:UCA→抑制内皮细胞NF-κB→降低CXCL1→阻断MDSC募集。
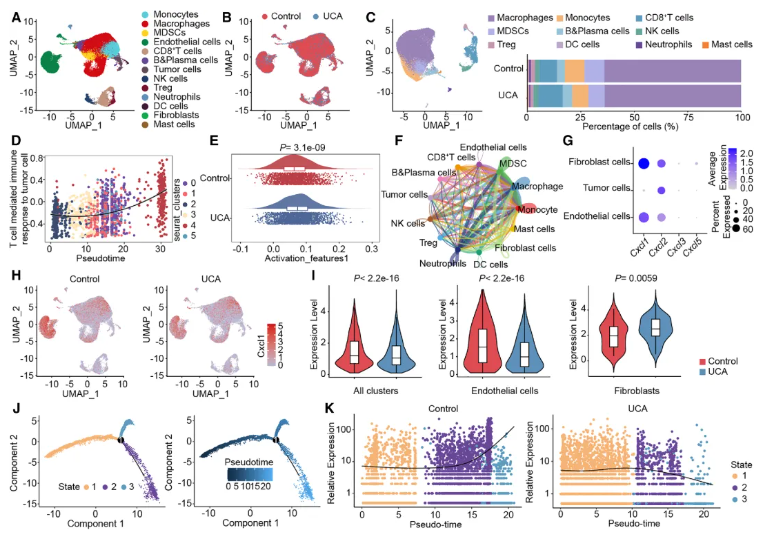
图4.UCA通过内皮细胞CXCL1调控TEC与MDSC之间的信号交流
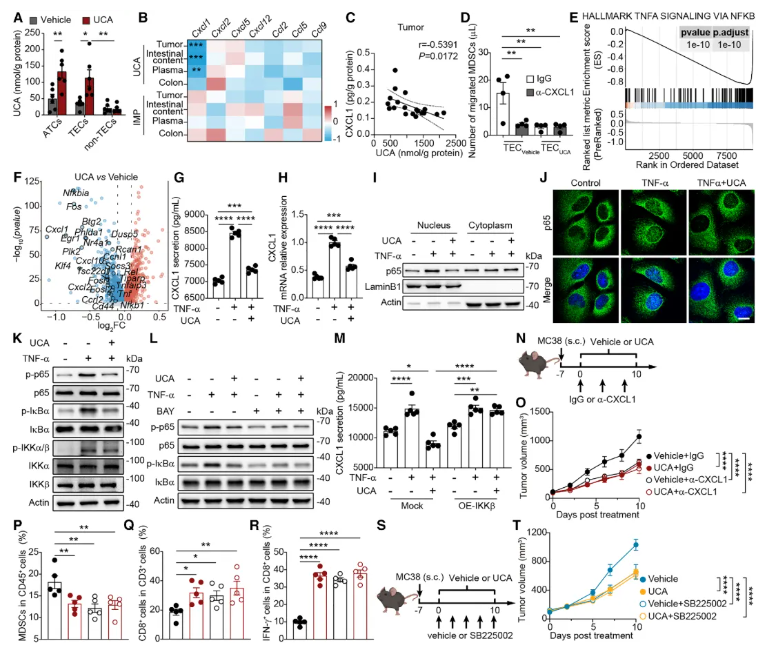
图5.UCA通过使内皮细胞NF-κB通路失活来抑制MDSC募集
05.精确打击:UCA直接结合IκBα,锁定关键位点
UCA究竟是如何精准地抑制NF-κB通路的?这需要找到它的直接作用靶点。研究人员设计并合成了一种带有生物素标签的UCA探针,利用它像 “钓鱼” 一样从细胞中钓出与UCA结合的蛋白质。质谱分析结果显示,这个靶点正是NF-κB通路的核心调控蛋白——IκBα。
IκBα是NF-κB的“枷锁”,在静息状态下结合并锁住NF-κB。当细胞受到刺激,IκBα的32位丝氨酸(Ser32)会被磷酸化,进而被降解,释放NF-κB入核发挥功能。那么,UCA是如何作用于IκBα的?通过高分辨率质谱与分子模拟,团队发现了一个全新机制:UCA与IκBα的第31位天冬氨酸(Asp31)发生共价结合(图6A–B)。这种结合使IκBα构象更紧凑、遮蔽Ser32位点,特异性阻断Ser32磷酸化,但不影响邻近的Ser36位点(图6F–J)。这种 “外科手术刀” 般的精准调控,让IκBα更加稳定,NF-κB通路因此被牢牢抑制。
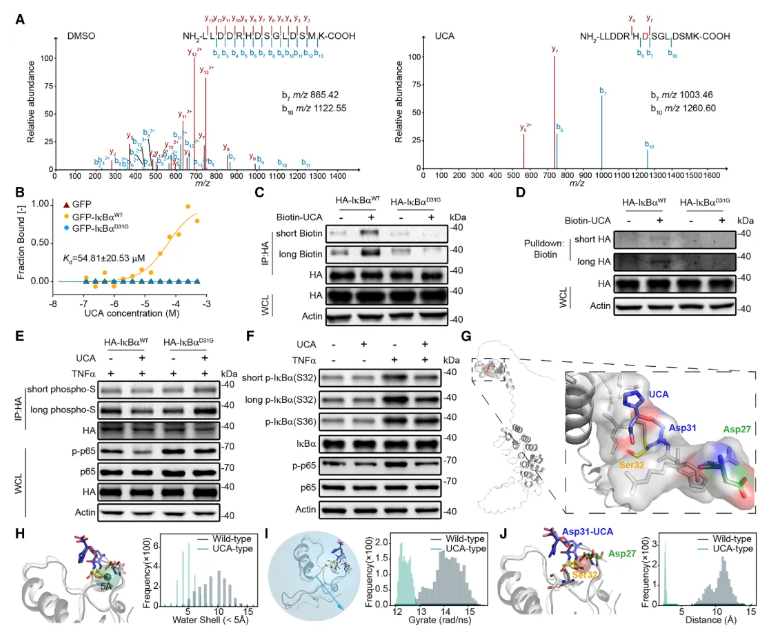
图6.UCA直接靶向IκBα,选择性抑制Ser32残基的磷酸化
06.临床应用:UCA增效PD-1,化身疗效预测“生物标志物”
以上发现是否具有临床转化价值?团队在两种不同的结直肠癌小鼠模型中进行了验证。结果显示,UCA与抗PD-1抗体联合使用,产生了显著的协同增效作用,肿瘤抑制效果远超单独用药,小鼠生存期显著延长(图7A–I)。在人源化小鼠模型中,TKIs处理同样能提升UCA水平,并增强抗PD-1的效果(图7O–Q)。
最后,团队回顾性分析了接受免疫治疗的结直肠癌患者临床样本。结果与动物实验高度一致:对抗PD-1治疗有响应的患者,其治疗前粪便中的Muribaculum gordoncarteri丰度和UCA水平均显著高于无响应者(图7R–S)。更重要的是,这些指标与患者的总生存期正相关,与肿瘤中MDSC的密度负相关,与CD8+ T细胞密度正相关(图7T–W)。这表明,粪便中Muribaculum gordoncarteri丰度和UCA浓度,有望成为预测免疫疗法疗效的全新、无创生物标志物。
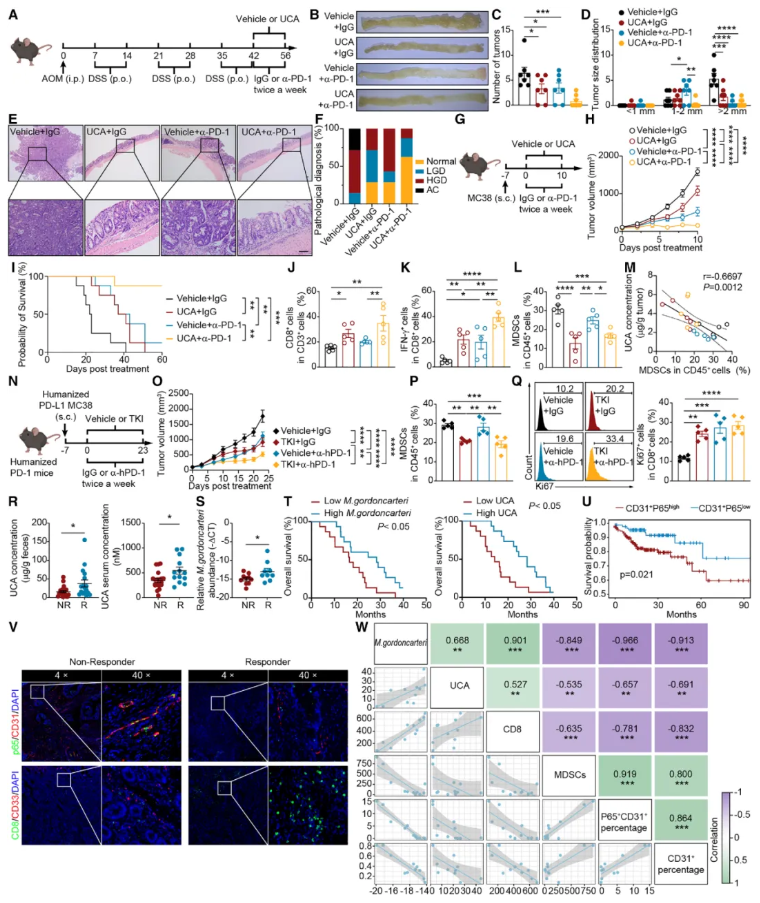
图7.M. gordoncarteri 来源的UCA可促进结直肠癌小鼠模型的免疫治疗反应并预测患者预后
研究总结
本研究揭示了一个全新的肠道菌-代谢物-宿主信号轴:酪氨酸激酶抑制剂诱导Muribaculum gordoncarteri产生尿刊酸(UCA),UCA通过靶向IκBα抑制NF-κB活化、降低CXCL1介导的MDSC募集,从而显著增强抗PD-1免疫治疗效果。UCA与Muribaculum gordoncarteri水平可作为免疫治疗疗效预测的潜在生物标志物,为联合靶向治疗及微生态干预提供了新策略。
