
文章标题:VRAC coordinates the trade-off between nutrient absorption and antimicrobial defense in enterocytes against inflammation
发表期刊:nature communications
影响因子:15.7
客户单位:南方医科大学
百趣提供服务:AQ700(现升级为AQ1100高通量靶标定量)
研究背景
炎症性肠病(IBD)是一类反复发作的慢性胃肠道疾病,同时也是炎症相关结直肠癌(CAC)的重要危险因素。目前,炎症性肠病的确切发病机制尚未完全阐明。
哺乳动物细胞需通过离子通道与转运蛋白转运离子及小分子有机渗透溶质,调控细胞体积,以应对渗透压变化引起的细胞肿胀或收缩。容积调控性阴离子通道(VRAC)可在细胞肿胀时介导氯离子外流,在恢复细胞正常体积的过程中发挥关键作用。肠上皮细胞持续暴露于渗透压波动中,但其内的VRAC在肠道炎症中的作用仍不明确。本研究发现,肠上皮细胞中的VRAC是肠细胞功能平衡的关键调控分子,可在炎症状态下协调营养吸收与抗菌防御之间的权衡,进而维持肠道内环境稳态。
研究结果
01.肠道VRAC功能缺失加剧结肠炎与炎症相关结直肠癌进展
本研究利用野生型(WT)与Lrrc8aΔIEC小鼠构建DSS诱导的结肠炎模型。相较于WT小鼠,经DSS处理后,Lrrc8aΔIEC小鼠体重下降更为显著,疾病活动指数(DAI)明显升高(图1A-B);敲除小鼠结肠长度显著缩短,提示其肠道炎症损伤更为严重(图1C)。3%DSS造模条件下,Lrrc8aΔIEC小鼠死亡率大幅上升(图1D)。组织学结果显示,DSS处理后,敲除小鼠肠道上皮糜烂、炎性浸润程度显著加重,分泌黏液的杯状细胞数量明显减少(图1E-F)。
同时,DSS造模后,髓系细胞特异性敲除组与T细胞特异性敲除组小鼠,在体重下降、DAI、结肠缩短及组织病理损伤方面均与对照组无显著差异(图1G–L),说明发挥保护作用的是肠上皮细胞VRAC,而非免疫细胞VRAC。
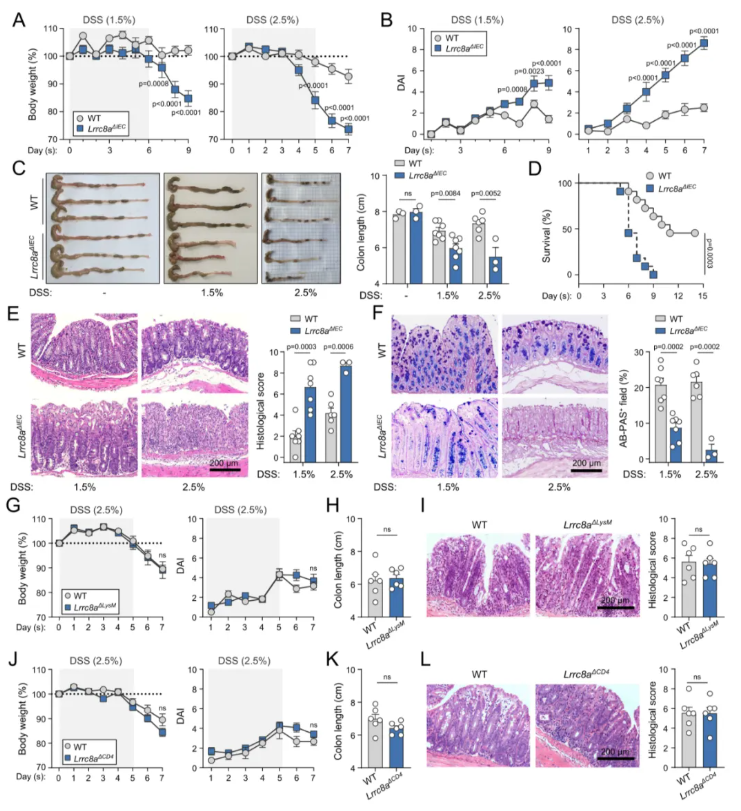
图1.肠道上皮细胞LRRC8A缺失加重DSS诱导的结肠炎
在此基础上,进一步探究VRAC对炎症相关结直肠癌的影响,采用AOM DSS联合诱导模型。结果显示,DSS处理期间,Lrrc8aΔIEC小鼠体重下降同样更为显著(图2A);AOM注射后第80天(模型终点),敲除小鼠结肠肿瘤负荷显著升高,表现为肿瘤数量更多、体积更大(图2B–D)。组织学检测进一步证实,Lrrc8aΔIEC小鼠肠道炎症范围更广、上皮增生程度更严重(图2E–G)。
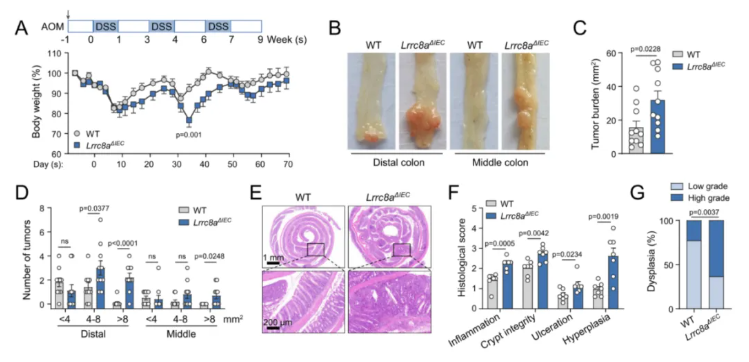
图2.肠道LRRC8A缺失加剧炎症相关性结直肠癌
02.Lrrc8aΔIEC小鼠表现出炎症反应增强和肠上皮损伤
本研究取DSS造模后的WT与Lrrc8aΔIEC小鼠结肠组织开展转录组测序分析。结果显示,与WT相比,Lrrc8aΔIEC小鼠共有110个基因显著下调、355个基因显著上调(图3A)。利用Enrichr数据库进行基因本体(GO)富集分析发现,Lrrc8aΔIEC小鼠体内炎症反应、中性粒细胞迁移、抗菌应答相关基因显著上调;而脂质转运、离子转运相关基因则明显下调(图3B)。经qPCR验证,在DSS或AOM DSS处理条件下,Lrrc8aΔIEC小鼠炎症相关基因表达水平显著升高,钙卫蛋白亚基S100a8、S100a9等抗菌肽相关基因表达也显著上调(图3C–E)。TUNEL染色结果提示 Lrrc8aΔIEC小鼠肠道细胞凋亡水平增加,上皮细胞增殖能力下降,表明肠道损伤修复功能受损(图3F)。Lrrc8aΔIEC小鼠结肠组织的紧密连接结构显著紊乱(图3G),提示该类小鼠黏膜屏障功能受损;血清荧光强度显著升高,进一步证实其存在结肠屏障渗漏(图3H)。
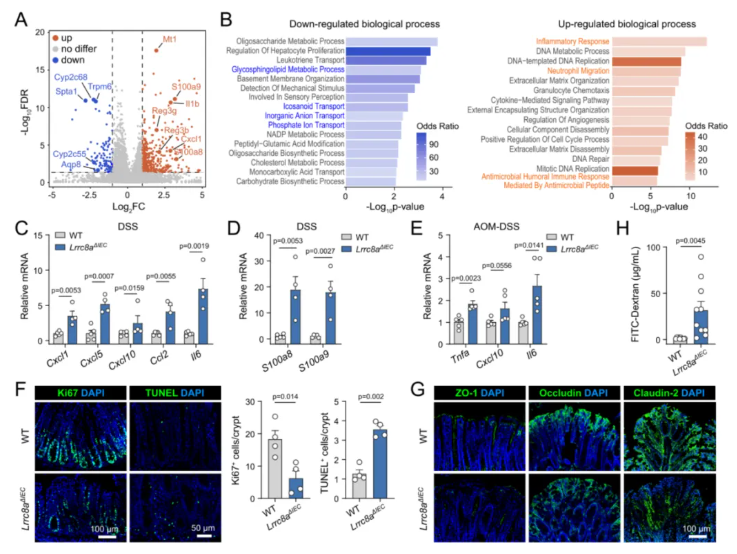
图3.肠道上皮细胞LRRC8A缺失会增强炎症反应并削弱DSS诱导结肠炎后的肠道再生修复能力
03.肠道VRAC特异性调控肠上皮肠细胞的成熟与功能分区
为阐明肠上皮细胞VRAC抵御肠道炎症的潜在分子机制,本研究发现LRRC8A主要表达于肠细胞与杯状细胞中(图4A–B)。与GEO公共数据库分析结果一致,LRRC8A与LRRC8D是人类肠上皮细胞中构成VRAC的主要功能亚基(图4B)。此外,与健康人群相比,结肠炎患者肠细胞中LRRC8A与LRRC8D的表达水平显著上调(图4C)。DSS造模后,相较于野生型小鼠,Lrrc8aΔIEC小鼠结肠组织中成熟肠细胞标志物的表达显著下调(图4D)。
沿结肠隐窝–腔面轴分布的肠细胞具有空间有序的功能分区特征,随着细胞向肠腔表面迁移,逐步获得各类代谢与营养吸收能力(图4E)。在DSS炎症刺激下,肠上皮VRAC缺失会破坏肠细胞的正常分区模式:肠细胞从中-上部吸收型特征向隐窝底部抗菌型特征偏移,表现为抗菌肽与金属离子转运体相关基因显著上调(图4E–F)。
相较于WT对照组,Lrrc8aΔIEC类器官中肠细胞标志物Alpi的表达显著降低;而干细胞标志物Lgr5与杯状细胞标志物Muc2在两种基因型间无明显差异(图4G)。在类器官中过表达LRRC8A可抑制Alpi表达;在Lrrc8aΔIEC类器官中回补LRRC8A,免疫荧光与qPCR结果均证实Alpi表达得以恢复(图4H)。
依据基因表达谱,所有细胞被划分为10个独立细胞亚群;结合经典细胞特异性标志物,进一步归类为6大主要细胞类群(图4I)。LRRC8A缺失可诱发肠细胞功能分区重塑,表现为隐窝底部肠细胞特征基因上调、中-表层肠细胞特征基因下调(图4J)。单细胞测序进一步显示,Lrrc8aΔIEC小鼠体内Reg3g+抗菌型肠细胞显著增多,而负责营养吸收的Nt5e+表层肠细胞明显减少(图4K)。
Lrrc8aΔIEC小鼠结肠组织及类器官中,BMP2、BMP7介导的BMP信号通路活性显著受抑(图4L)。此外,外源性补充肠道关键BMP配体BMP2,可显著恢复Lrrc8a^ΔIEC类器官中成熟肠细胞标志物Alpi的表达(图4M)。
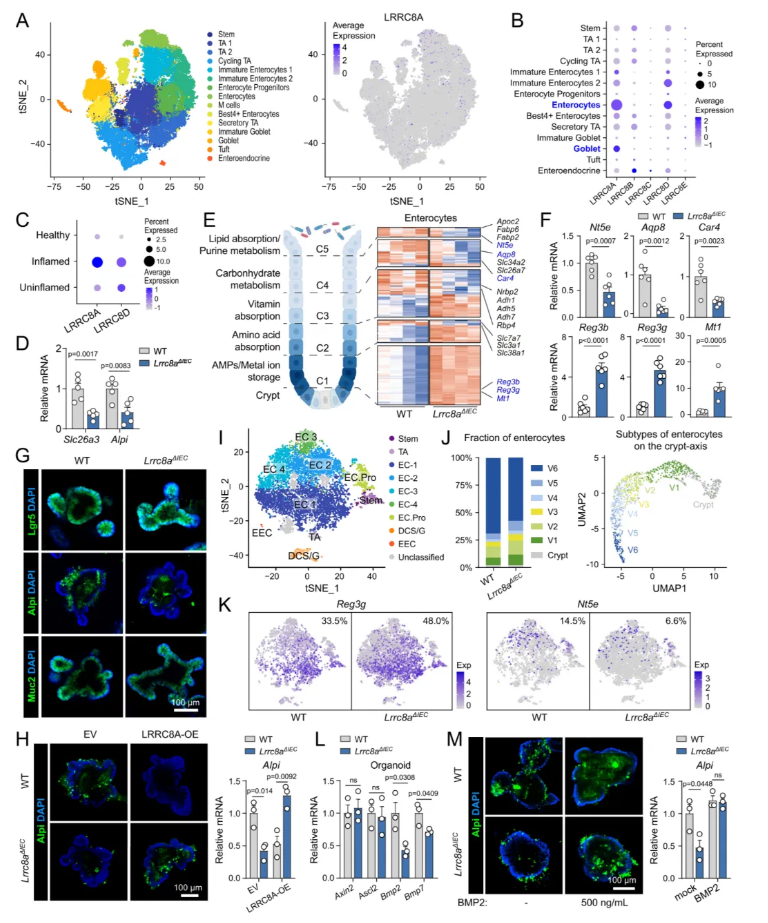
图4.VRAC协调调控吸收型肠细胞的空间分区分化
04.VRAC通过调控视黄酸代谢抵御肠道炎症
本研究利用DSS造模后WT与Lrrc8aΔIEC小鼠的转录组测序数据进行IPA通路分析。IPA核心分析结果显示,排名前十的下调经典通路中,有四条与视黄酸(RA)信号通路密切相关(图5A)。已有研究证实,RA可通过激活RA受体(RARs)及类视黄醇X受体(RXRs),在调控肠道上皮功能与肠道免疫中发挥多重生物学作用(图5B)。VRAC缺失的肠道上皮细胞中,Adh1、Aldh1a1、Aldh1a2表达显著下调;而Rdh7与RA降解基因Cyp26a1在WT与Lrrc8aΔIEC之间均呈低表达、无明显差异,Lrrc8aΔIEC小鼠肠道上皮中RA应答基因Nos2的表达亦显著降低(图5C)。
本研究在DSS造模前对小鼠预防性灌服全反式视黄酸(atRA)(图5D)。结果显示,atRA预处理可有效缓解肠上皮细胞VRAC缺失所加剧的肠道炎症:敲除小鼠的结肠长度、组织学评分及AB PAS染色指标均得到明显改善(图5D–G)。同时,经atRA干预后,WT与Lrrc8aΔIEC小鼠肠道上皮中RA合成酶的表达水平与ALDH酶活性恢复至相近水平(图5H–I)。此外,atRA处理可显著逆转Lrrc8aΔIEC类器官中成熟肠细胞标志物Alpi的低表达状态(图5J)。
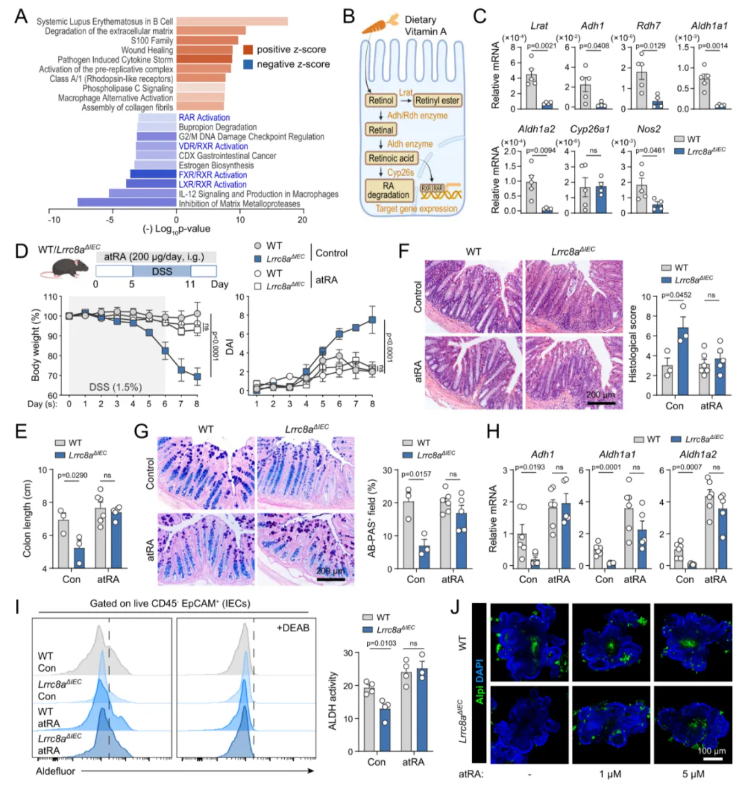
图5. 补充RA可逆转上皮VRAC缺失所诱发的肠道炎症加重
05.肠道上皮VRAC缺失会抑制Th17与ILC3s细胞分泌IL-17及IL-22
鉴于IL 17A与IL 22在维持黏膜屏障完整性中发挥关键作用,本研究进一步分析了两类细胞因子的分泌细胞亚群。结果表明,Lrrc8aΔIEC小鼠体内分泌IL 17A/IL 22的Th17细胞与ILC3细胞数量显著减少;atRA处理可显著恢复敲除小鼠结肠固有层中 IL 17A⁺/IL 22⁺Th17细胞与ILC3细胞的比例,证明外源性atRA可有效逆转上皮VRAC缺失引发的免疫功能缺陷(图6A–D)。
为阐明肠道上皮VRAC缺失对免疫细胞应答的调控机制,本研究收集Caco 2WT与Caco 2ΔLRRC8A细胞培养上清开展体外功能实验。中性粒细胞对两种细胞上清的应答无明显差异;但Caco 2ΔLRRC8A细胞的培养上清可显著抑制Th17细胞与ILC3细胞中IL 17、IL 22阳性细胞比例(图6E–F)。
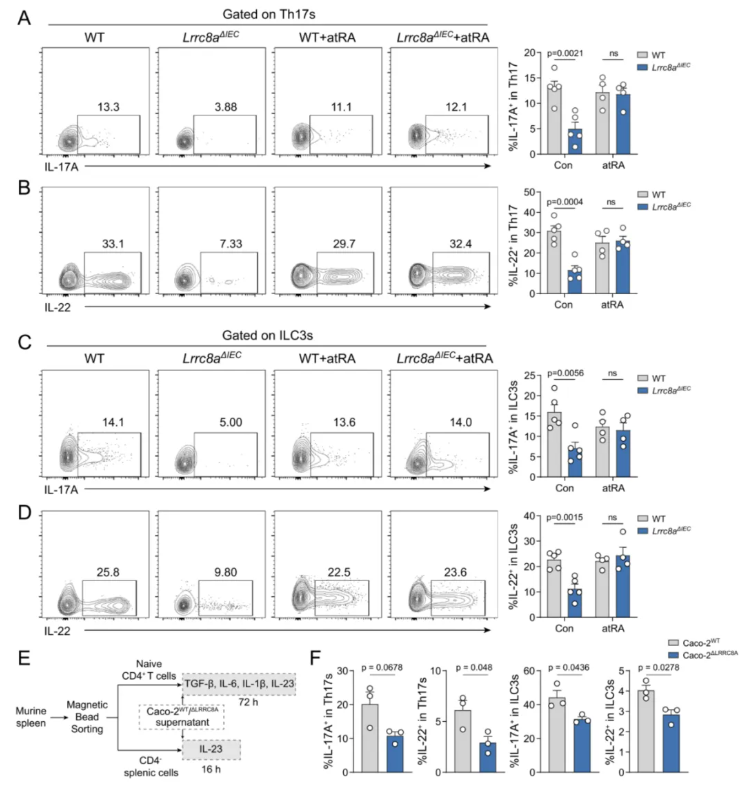
图6.RA可恢复Lrrc8aΔIEC小鼠体内受损的IL 17A⁺和IL 22⁺淋巴细胞亚群
06.VRAC缺失通过肠道微生物群依赖性方式驱动肠道炎症
本研究将WT与Lrrc8aΔIEC同窝小鼠共同饲养4周,再给予DSS造模。结果显示,共同饲养可消除两种基因型小鼠在DSS诱导性结肠炎严重程度上的差异(图7A–D)。将Lrrc8aΔIEC小鼠的粪便菌群移植至抗生素预处理的受体小鼠后,受体小鼠经DSS诱导出现更为严重的结肠炎(图7E–H)。随后,本研究对DSS处理后、有无atRA干预条件下的WT与Lrrc8aΔIEC同窝小鼠粪便样本开展16S rRNA测序。结果显示,敲除小鼠肠道菌群的微生物多样性与物种丰富度均显著下降(图7I–J)。此外,基于Bray–Curtis相异系数的主坐标分析结果显示,各组间β多样性存在明显差异,WT对照组与Lrrc8aΔIEC小鼠菌群各自独立聚类(图7K)。Lrrc8aΔIEC小鼠的乳杆菌在属和物种层面的丰度均显著降低(图7L–M);补充RA能够显著恢复乳杆菌丰度,并下调Reg3b、Reg3g等抗菌肽的表达(图7N–O)。
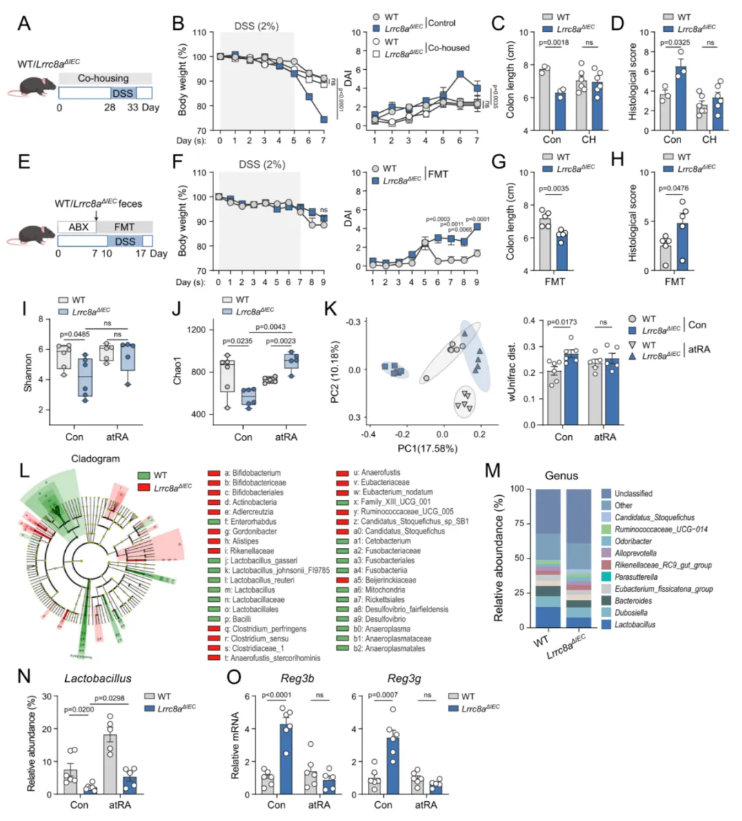
图7.肠道菌群介导了Lrrc8aΔIEC小鼠在实验性结肠炎中的有害病理表型
07.补充乳杆菌可缓解Lrrc8aΔIEC小鼠的重症肠道炎症
结合前文实验结果,乳杆菌是Lrrc8aΔIEC小鼠体内缺失最显著的有益菌。本研究选取鼠乳杆菌与罗伊氏乳杆菌两种菌株开展干预实验。结果显示,单独补充任一乳杆菌菌株,均可显著缓解上皮VRAC缺陷导致的肠道炎症:小鼠体重下降幅度、DAI、结肠长度及组织学损伤评分等炎症相关指标均得到明显改善(图8A–E)。
在Lrrc8aΔIEC小鼠中,补充鼠乳杆菌可显著上调肠道上皮细胞中Adh1与Aldh1a2的表达,使其恢复至WT水平(图8F)。同时,两种乳杆菌菌株干预均可有效恢复上皮ALDH酶活性、纠正组织抗菌肽异常表达,并回升结肠固有层中IL 17A⁺与IL 22⁺淋巴细胞亚群比例(图8F–H)。
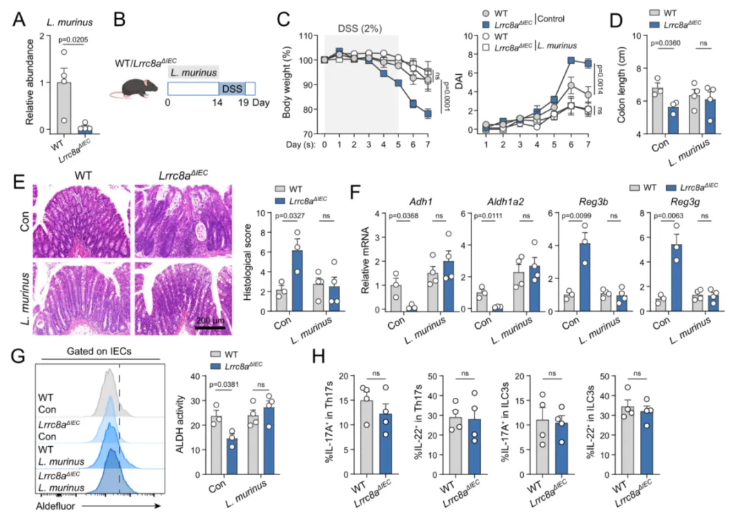
图8. 补充乳杆菌可缓解Lrrc8aΔIEC小鼠的重症肠道炎症
研究总结
本研究体内外实验共同证实,VRAC缺失会特异性破坏肠细胞的成熟与空间分区模式。Lrrc8aΔIEC小鼠中,抗菌肽分泌型肠细胞显著增多,营养吸收型肠细胞明显减少。适度向抗菌防御倾斜的细胞分区重塑可帮助机体抵御肠道炎症;但过度偏移会严重削弱营养吸收能力,破坏肠道上皮完整性与黏膜免疫稳态。与此同时,抗菌肽过量分泌会抑制有益菌定植,形成炎症恶性循环。维持营养吸收与抗菌防御的动态平衡是肠道稳态的核心,而VRAC可作为肠道上皮的关键调控变阻器,在炎症环境中精细校准二者平衡,维系肠道生理稳态。
