
英文标题:Spatially Resolved Multiomics: Data Analysis from Monoomics to Multiomics
中文标题:空间分辨多组学:从单组学到多组学的数据分析
发表期刊:BME Frontiers
影响因子:7.7
文章简介
为促进生物学研究及精准医疗领域发展,中国科学院苏州生物医学工程技术研究所周连群研究员、张威研究员团队在Science合作出版的期刊BME Frontiers上发表题为“Spatially resolved multiomics: data analysis from monoomics to multiomics”的综述文章,总结了空间单组学技术的发展及其数据分析流程的改进,提出基于空间单组学技术的空间多组学数据整合策略,涵盖跨平台、跨切片和跨模态整合,旨在助力研究人员和临床医生更好地理解这些技术的进展。
技术路线
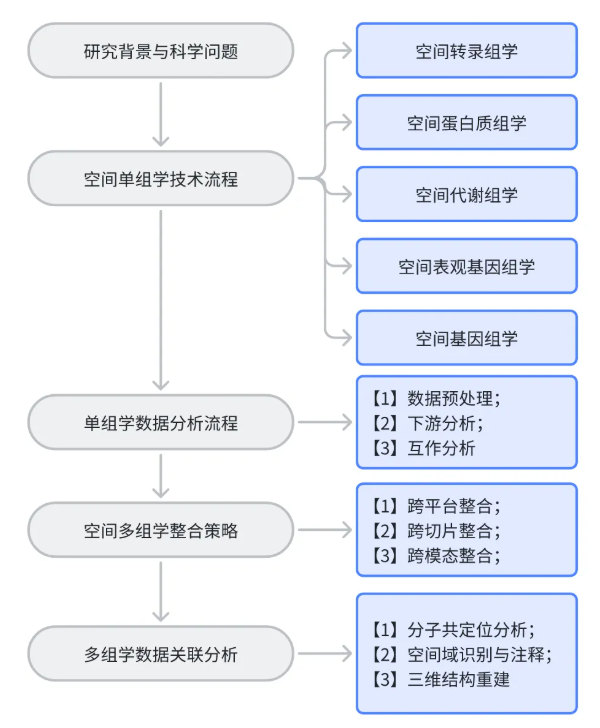
研究结果
1、空间组学技术分类与核心技术
空间转录组学是指在组织内对转录本进行定位和定量分析的技术,旨在探究基因表达的空间分布规律,揭示细胞功能与组织微环境的关系。它主要分为基于图像和基于空间条形码的两类技术,具体分类如下:
a)基于图像的空间转录组技术:原位杂交(ISH)、单分子荧光原位杂交(FISH)、顺序荧光原位杂交(seqFISH)、多重误差稳健荧光原位杂交(MERFISH)、原位测序(ISS)、荧光原位测序(FISSEQ)技术、扩展测序(ExSeq)技术、Xenium技术(可同时检测高通量转录本与低通量蛋白质,达单细胞分辨率);
b)基于空间条形码的转录组技术:VisiumHD(空间分辨率2μm)、Slide-seq(10μm编码微球,达单细胞分辨率)、空间增强分辨率组学测序(Stereo-seq,分辨率0.22μm,支持大组织分析)、确定性组织条形码测序(DBiT-seq,微流控原位标记,无法实现单细胞分辨率)(图1A)。
空间蛋白质组学用于检测组织中特定蛋白质抗原的空间分布与丰度,主要包含:a)质谱流式细胞术(MC):包括成像质谱细胞术(IMC)和多重离子束成像(MIBI);b)多重免疫组织化学(mIHC)(图1B)。
空间代谢组学将质谱成像(MSI)与代谢组技术相结合,能够在组织切片上逐像素检测内源性代谢物和外源性药物,并获取空间位置信息。MSI技术根据离子源的不同可分为以下类别:基质辅助激光解吸/电离质谱成像(MALDI-MSI)、二次离子质谱成像(SIMS-MSI)、解吸电喷雾电离质谱成像(DESI-MSI)(图1C)。
空间基因组学主要研究多细胞生物体内特定组织或器官中,不同细胞类型在特定位置的基因组序列及其在细胞核中的空间分布随时间的变化规律,目前核心技术为Slide-DNA-seq(图1D)。
空间表观基因组学聚焦基因组表观修饰的空间分布,主要包含:Spatial-CUT&Tag技术(基于pA-Tn5转座体,分析全基因组蛋白修饰图谱);Spatial-ATAC-seq技术(结合微流控二维编码,分析全基因组染色质可及性)(图1E)。
空间多组学技术通过两片微流控芯片(Group A/B 形成二维坐标系),开发出基于空间条形码的多功能多组学分析框架。目前可实现空间多组学数据检测的技术包含:空间ATAC-RNA-seq技术;空间CUT&Tag-RNA-seq技术;DNA-seqFISH+、DNA-MERFISH;NanoString GeoMx数字空间图谱技术;空间CITE-seq(图1F)。
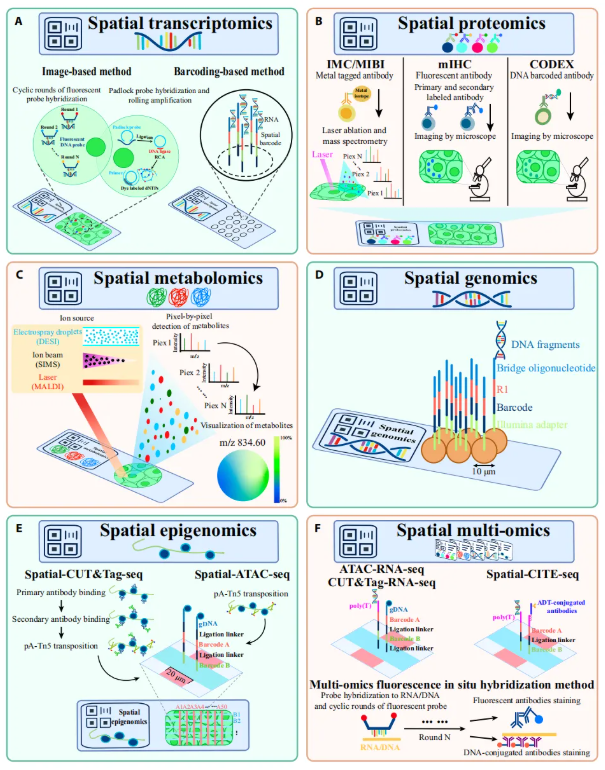
图1. 空间组学的示意图概要
2、空间单组学的数据分析流程
研究系统梳理了空间转录组学、空间蛋白质组学、空间代谢组学、空间基因组学、空间表观基因组学的数据分析流程(总览见图2A),核心步骤如下:
空间转录组学:
预处理:分技术类型生成矩阵——图像类(如seqFISH+)经图像去噪、细胞分割得“基因-细胞-图像矩阵”;条形码类(如Stereo-seq)经序列过滤(Trimmomatic)、基因组比对(STAR)得“基因-斑点坐标矩阵”(图2B)。
细胞类型鉴定:图像类用“特征鉴定(PCA+聚类)”或“scRNA-seq映射(Tangram)”;条形码类用“反卷积+scRNA-seq(SPOTlight/Cell2location)”。
下游分析:空间聚类(BayesSpace/SpaGCN)、邻域分析(HistoCAT)、细胞通讯(SpaTalk/COMMOT,基于配体-受体互作)(图2C)。
空间蛋白质组学:
含预处理(质谱类基线校正/峰提取,图像类去模糊/细胞分割)、细胞类型鉴定(PhenoGraph/MAP,依赖marker抗体)、邻域分析(Cytomap)、功能组织区域分析(TissueSchematics组装细胞邻域为高阶功能区)(图2D)。
空间代谢组学:
含预处理(峰对齐、TIC归一化、METASPACE注释)、单变量分析(t检验/Mann-Whitney U检验,火山图可视化)、多元分析(PCA降维、PLS-DA/OPLS-DA分组,置换检验防过拟合)(图2E)。
空间基因组学:
含预处理(序列比对、TSS富集评分计算)、克隆区鉴定(KNN平滑+PCA+k-means,Calinski-Harabasz指数选最优k)、基因组区域富集分析(500次置换检验,识别遗传异常)(图2F)。
空间表观基因组学:
含预处理(Snakemake重格式化、MACs2峰识别)、评分模型(ArchR计算基因score)、scRNA-seq联合分析(FindTransferAnchors对齐注释细胞类型)、拟时序分析(addTrajectory函数揭示分化路径)(图2G)。
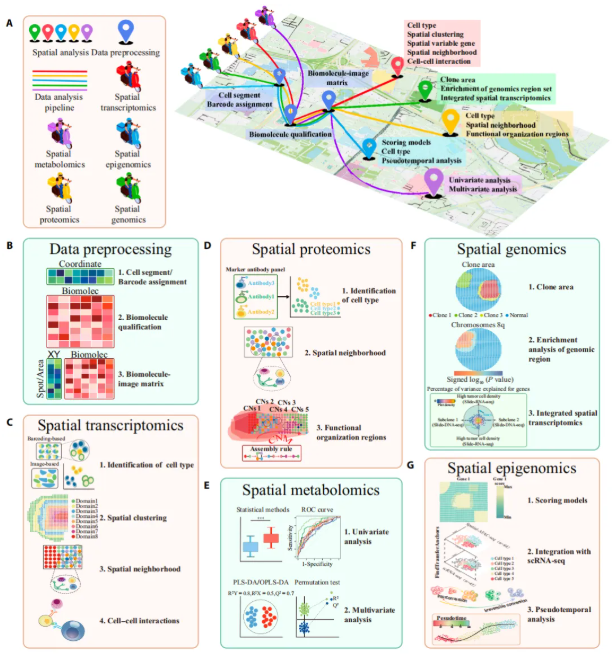
图2. 空间单组学数据分析流程
3、空间多组学的数据分析
与技术成熟的单细胞多组学领域相比,空间多组学技术仍处于发展初期,目前缺乏成熟的数据分析流程与标准化整合策略。本文中,研究人员重点梳理了空间多组学的数据分析核心流程,并提出适用于其数据的整合策略,核心模块包括数据存储、数据预处理、数据整合、数据相关性分析(含相同空间域识别、三维重建等子方向),同时补充了方法性能的验证指标(整体流程见图3)。
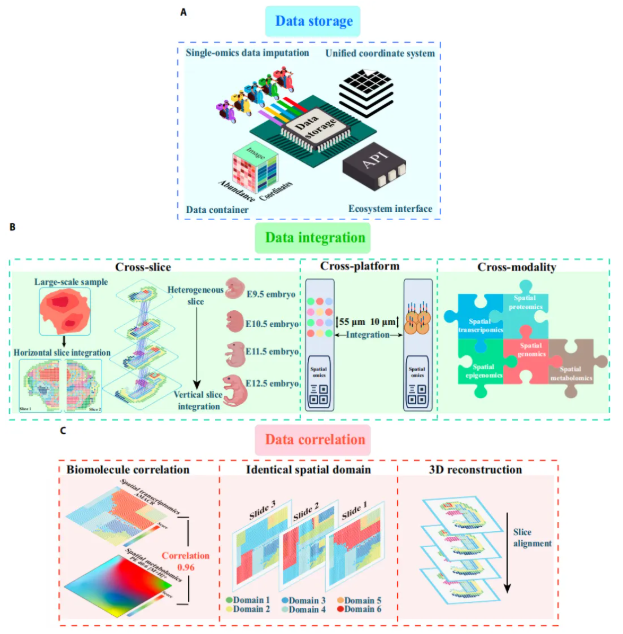
图3. 空间多组学数据分析流程
4、空间组学技术的应用
研究人员对空间组学(含单组学与多组学)在肿瘤、罕见病、人类细胞图谱(HCA)和人类生物分子图谱计划(HuBMAP)、药物发现、发育生物学、精准医学领域的应用进行系统总结,主要内容如下:
1)肿瘤领域应用:肿瘤微环境(TME)由肿瘤细胞、免疫细胞、基质细胞、成纤维细胞、细胞外基质和血管组成。空间多组学技术可整合生物分子及其物理空间位置,系统推动肿瘤研究,具体包括解析TME细胞分布(如乳腺癌中iCAFs富集于免疫基质区)、揭示肿瘤代谢重编程(如胃癌界面区谷氨酰胺代谢差异)、绘制肿瘤克隆进化图谱(如前列腺癌拷贝数变异空间分布)(图4A)。
2)罕见病领域应用:罕见病给全球公共卫生带来巨大挑战(图4B)。目前许多罕见病机制不明,治疗方案低效且并发症风险高,而空间多组学技术为解决这些问题提供了新思路——如通过Stereo-seq发现特发性多中心Castleman病(iMCD)中NCOA4/TRAF3功能异常,通过空间蛋白质组学揭示遗传性感觉自主神经病9(HSAN9)中TECPR2截断对神经蛋白运输的影响。
3)人类细胞图谱(HCA)和人类生物分子图谱计划(HuBMAP):随着多组学技术进步,HCA与HuBMAP计划已启动(图4C)。这些计划旨在构建非疾病人类器官的空间多组学图谱,为理解人类健康、疾病诊断与治疗奠定基础,而空间多组学技术正成为完成这些任务的核心工具。
4)药物发现领域应用:药物靶点发现、药物筛选和药代动力学是医学工程的重要任务,空间组学技术在此中发挥关键作用(图4D):空间基因组学可在单细胞分辨率下分析目标区域基因表达,精准识别靶点(如发现MAPK信号促进肿瘤发展);空间代谢组学可评估药物在组织中的分布(如结核兔模型中利福平比利福喷丁更易穿透空洞病变)。
5)发育生物学领域应用:技术瓶颈曾限制对人类胚胎关键发育事件的研究,而空间单组学技术的突破或将开启“黑箱”研究——其可精准定义细胞功能状态与发育轨迹,捕获细胞时空演化,例如解析人类肺胚胎中GRP+/GHRL+神经内分泌细胞分化、人类心脏胚胎不同解剖区域基因表达模式、小鼠脑发育中Pax6-Eomes-Tbr1调控级联(图4E)。
6)精准医学领域应用:随着深度学习与机器学习在基因研究中的突破,AI技术已用于辅助病理学家基于病理切片进行临床诊断,研究人员还可运用机器学习精准delineate肿瘤区域(如基于乳腺癌转录组训练模型分类肿瘤区域)(图4F)。此外,空间技术还能监测疾病进展(如Spatial iTracer追踪脑类器官细胞命运克隆性),Spatial-CITE-seq结合诊断标志物(如TTF1、p63)与免疫标志物(如PD-L1、CD8),可优化免疫治疗策略。
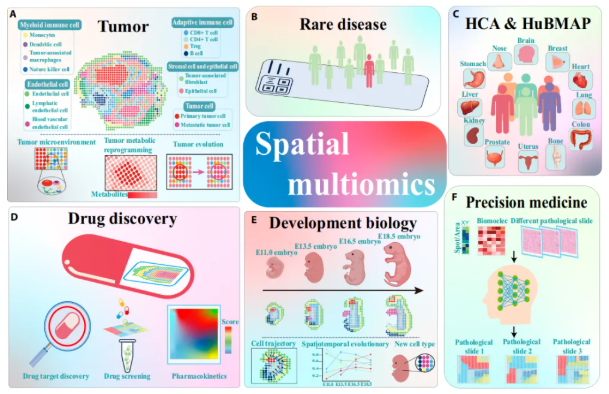
图4. 空间组学技术的应用
研究结论
本研究系统探讨空间单组学与多组学技术的最新进展,涵盖技术手段、数据分析流程及转化应用,着重强调数据分析的重要性,系统梳理了空间单组学从数据预处理到下游分析的完整流程,并针对空间多组学缺乏成熟分析策略的挑战,提出跨平台、跨切片、跨模态的整合策略,概述了完整的多组学数据分析流程,为生物医学研究与精准医疗发展提供了关键技术与方法支持。
百趣生物空间代谢组学,通过离子源(MALDI/DESI/SIMS)直接扫描生物样品成像,可以在同一张组织切片同时分析数百种甚至数千种代谢物的空间分布特征,从而对代谢物进行定性、定量、定位三个维度的分析。
百趣生物空间转录组学,通过对样本包埋切片并与检测芯片结合,利用序列标签(spatial barcode和UMI)区别不同细胞的空间位置,可高效检测组织中空间原始位置上的基因表达模式,两者联合可同时获取细胞类型、功能及空间定位信息。
百趣生物空间蛋白组学,可实现 “单细胞级别” 精准分析,其以高精度激光捕获显微切割技术(LCM)为核心,结合超微量蛋白无损提取、酶切及高灵敏度质谱分析,实现不同空间位置蛋白表达的精准检测。该技术可精确识别特定组织区域与细胞类型,为研究细胞空间异质性、解析细胞微环境复杂性提供有力工具,助力疾病机制研究与新型生物标志物发现。