
英文标题:Shared and disease-specific pathways in frontotemporal dementia and Alzheimer’s and Parkinson’s diseases
中文标题:额颞叶痴呆、阿尔茨海默病和帕金森病的共有通路及疾病特异性通路
发表期刊:nature medicine
影响因子:50
研究背景
阿尔茨海默病(Alzheimer’s Disease, AD)、帕金森病(Parkinson’s Disease, PD)和额颞叶痴呆(Frontotemporal Dementia, FTD)是最常见的神经退行性疾病,虽各有特定病理标志(如AD的淀粉样蛋白-β和tau蛋白、PD的α-突触核蛋白、FTD的tau蛋白等),但存在显著的临床和神经病理重叠(如19-57%的AD病例存在TDP-43病理,约20-30%的AD患者有α-突触核蛋白阳性),这给鉴别诊断和有效治疗的开发带来挑战。血浆蛋白质组学为研究这些疾病的全身性特征和外周变化提供了可能,不过现有研究多聚焦单一疾病,且FTD的血浆研究样本量小、测量蛋白少,缺乏对多种神经退行性疾病的大规模比较分析,尤其在蛋白组学相关性及分子机制的系统评估方面存在不足。因此,亟需通过大规模血浆蛋白组学数据,探究这些疾病的共享及特异性分子机制,以推动诊断和治疗策略的发展。
研究结果
1、患者、蛋白质组学数据及研究设计
本研究使用全球神经退行性疾病蛋白质组学联盟(GNPC)1.0版本的大型横断面血浆蛋白质组学数据集,含23个独立站点样本。GNPC资源共31,111份样本,来自21,979名患多种疾病的个体,其中1,638人因CDR>0.5或MMSE<19且无明确诊断被归为痴呆症。
本研究纳入临床诊断的AD、FTD、PD患者及认知正常对照者,对照者需CDR=0且MMSE≥24,AD患者需CDR>0,PD和FTD患者均经临床诊断,最终数据集含16个站点的10,527份样本,包括1,936例AD、525例PD、163例FTD、1,638例痴呆症和6,265例对照者(表1)。
采用SomaScan 4.1检测,量化7,595种适配体(靶向6,386种人类蛋白质),7,289种适配体通过质控。通过线性回归分析(校正年龄、性别和前两个蛋白质组学主成分)比较各疾病组与对照组,FDR<0.05的蛋白质为显著相关蛋白。还评估显著蛋白效应量的成对相关性,并进行细胞类型富集、通路及网络分析,以识别共同或独特失调的生物学过程及关键蛋白质(图1),从而系统理解AD、PD和FTD的蛋白质组学特征。
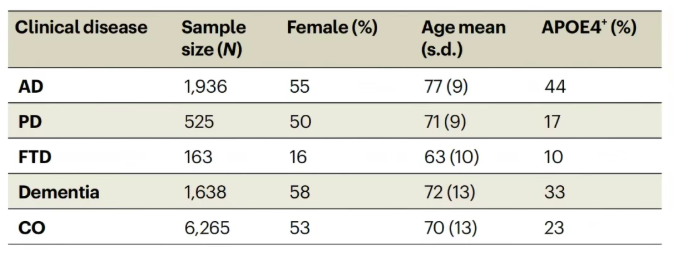
表1. 血浆采集时参与者的人口统计学信息
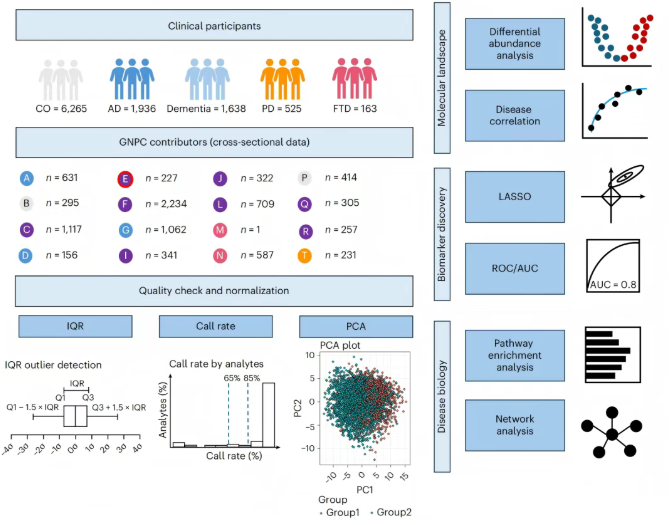
图1. 绘制神经退行性疾病中人类血浆蛋白质组的框架
2、神经退行性疾病间的血浆蛋白质组差异
分析7000多种蛋白质适配体发现,AD、PD、FTD分别与5187种(71%)、3748种(51%)、2380种(33%)蛋白质显著相关(图2)。研究验证了已知生物标志物(如AD中的YWHAH、SMOC1),并发现新蛋白质(如AD中的PRDX3、ENO2),其中AD存在独特的凋亡相关蛋白(如DSG1、CASP3),且相关蛋白质在内皮细胞和小胶质细胞/巨噬细胞中富集(图3);PD富集蛋白质降解和泛素化相关蛋白(如HGS、PARK7);FTD涉及tau病变相关蛋白(如MAPT)及泛素-蛋白酶体系统蛋白(如UBE2D1|UBB)。
跨队列分析表明,多数与疾病显著相关的蛋白质在不同研究队列中表达波动较小,稳定性较好。通过极端三分位数比较计算的比值比显示,AD、PD、FTD的平均比值比分别为1.61、2.39、5.08,提示这些蛋白质与疾病的关联强度存在差异,其中FTD相关蛋白质的关联最强。同时,关键蛋白质与疾病的关联在不同检测平台(如SomaScan、Olink等)上均表现出一致的趋势,验证了结果的可重复性。
此外,996种蛋白质(15.2%)为三种疾病共有(如SMOC1、NPTXR),AD与PD共享1664种(25.4%),AD与FTD共享691种(10.5%),PD与FTD共享415种(6.33%);AD的疾病特异性蛋白质最多(1836种,28%),其次为PD(673种,10.3%)和FTD(278种,4.24%)(图4a及图3b)。
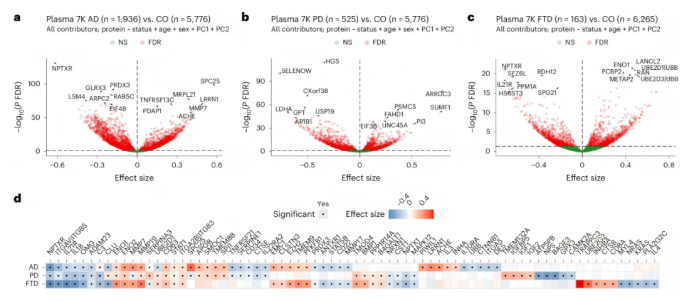
图2. 与对照组相比,AD、PD和FTD患者的血浆蛋白质组变化
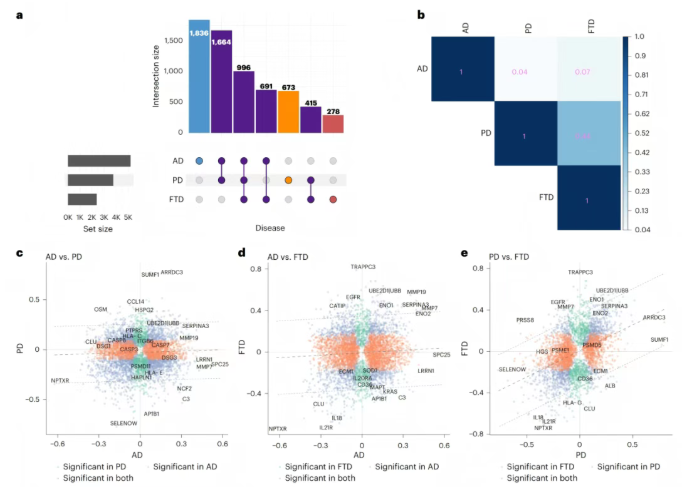
图3. 疾病相关蛋白质的重叠及细胞类型富集情况
3、神经退行性疾病中共享及疾病特异性分子变化的评估
研究通过成对相关性分析评估AD、PD、FTD相关蛋白质效应量的相似性,发现PD与FTD的蛋白质组学变化重叠最高,AD与PD重叠最低,AD与FTD重叠较低(图4b)。
进一步分析(图4c-e)显示,AD与PD的差异体现在部分蛋白质效应方向相反(如SPC25、LRRN1)或效应量差异显著(如SUMF1、HGS);AD与FTD的有限重叠由信号转导相关蛋白(如KRAS)驱动,但糖酵解相关蛋白(如ENO2)等存在一致变化;PD与FTD的共享机制涉及蛋白质降解(如UBE2D1|UBB)和神经炎症(如TRAPPC3、IL-18),但突触蛋白(如CLU、MMP7)效应方向相反。
综上,三种疾病虽有独特蛋白质组学特征,但存在蛋白质清除缺陷和突触功能障碍的共同机制。
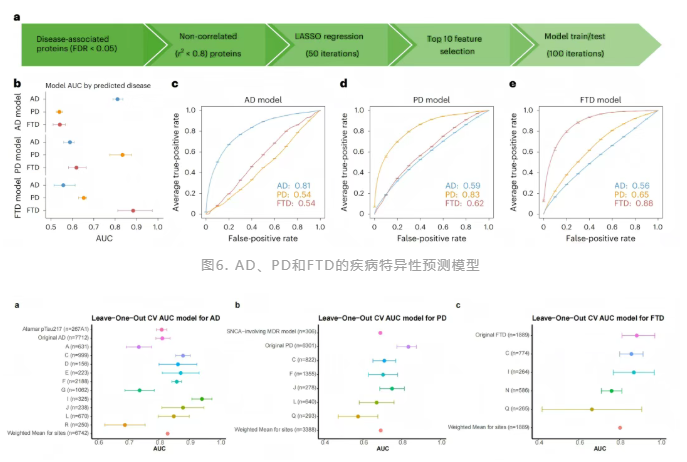
图4. 与AD、PD和FTD相关的蛋白质的重叠及效应量相关性
4、AD、PD和FTD中存在的差异性通路失调
为探究共有及疾病特异性蛋白质所指向的疾病相关生物学机制,研究对AD、PD和FTD中差异丰度的血浆蛋白质进行了通路富集分析(图5a)。
疾病特异性蛋白质(AD=1836种、PD=673种、FTD=278种)分别关联164、136和83条通路;不同疾病重叠蛋白质则关联不同数量的共有通路,其中三种疾病共有关联101条,PD与FTD关联最多(115条)(图3b)。
三种疾病均显著富集的通路包括“血小板活化、信号传导和聚集”“糖酵解”“免疫系统”及“细胞外基质组织”,涉及MMP家族、烯醇化酶(ENO1、ENO2)等关键蛋白质,体现免疫、能量代谢及基质重塑的共同异常。
AD特异性蛋白质富集于“细胞蛋白质的凋亡切割”等通路(涉及CASP3、ITGA5等),反映凋亡及血脑屏障损伤;PD特异性蛋白质富集于“内质网-吞噬体通路”等(涉及HLA蛋白、蛋白酶体);FTD则富集“白细胞介素信号传导”和“血小板脱颗粒”通路(涉及IL-2、SOD1等),提示血管因素的潜在作用。
综上,通路分析揭示了三种疾病在免疫、糖酵解等通路的共同失调,以及各自独特的病理生理特征,结合细胞类型关联可深化对神经退行性过程的理解。
5、上游调控因子和机制枢纽的网络分析
为探究蛋白质表达失调如何通过功能网络产生影响,研究利用AD、PD和FTD相关蛋白质构建了疾病特异性蛋白质-蛋白质相互作用(PPI)网络,并通过方向性网络建模识别上游调控因子及关键节点(图5b-d)。
AD特异性网络(图5b)以免疫调节等通路相关蛋白为核心,PSMB10、RPS27A和TAX1BP1为关键上游调控因子,调控VCP、IL-6R等下游靶标,涉及蛋白质降解和小胶质细胞活化。
PD网络(图5c)中,IRAK4作为TLR/IL-1信号通路核心激酶,直接关联PPP2R1A和RIPK1;FOXO3 则连接应激反应蛋白,而SNCA通过蛋白质稳态子网络与PTEN等关联,PTEN成为影响神经元韧性的中心枢纽。
FTD特异性网络(图5d)中,MAPK1作为上游调控因子直接调控MAPT等,其扰动可影响近三分之一网络蛋白;MAPT处于网络中心,ADAM10则连接炎症信号与突触功能障碍。
综上,网络分析揭示了AD中RPS27A、PD中IRAK4、FTD中MAPK1等关键调控蛋白,强调泛素化和激酶相关蛋白在三种疾病的蛋白质稳态、免疫信号等通路中的共同调控作用。
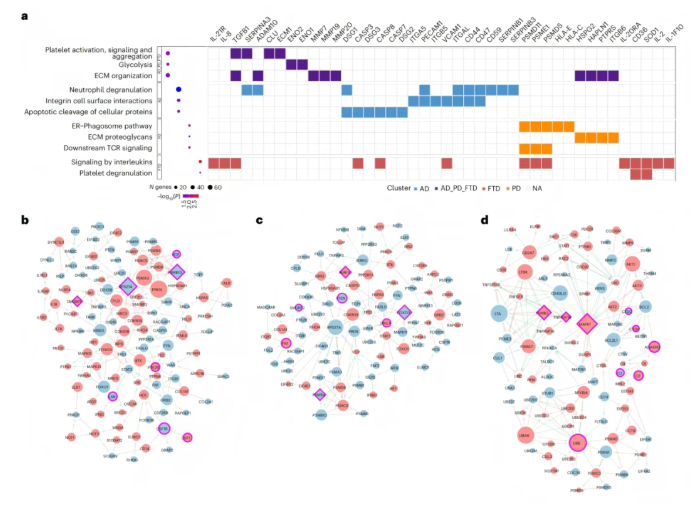
图5. AD、PD和FTD的通路富集及网络分析
6、疾病特异性生物标志物组合
为了区分AD、PD和FTD,研究用LASSO回归方法构建了基于血浆的预测模型。模型通过100次迭代训练,每次用70%的数据训练、30%的数据测试,且保证病例和对照在训练与测试中比例均衡(图6a)。
这些模型在区分每种疾病与健康人时效果较好:AD的曲线下面积(AUC)为0.81,PD为0.83,FTD为0.88(图6c-e)。但用这些模型去预测其他神经退行性疾病时,效果明显下降,体现了疾病特异性。比如,AD的生物标志物组合用来预测PD和FTD时,AUC都是0.54,接近随机猜测的水平;FTD的组合预测AD(AUC=0.56)和PD(AUC=0.65)时,效果也有限。这和不同疾病蛋白质组学的重叠程度有关,像PD和FTD的蛋白质变化更相似,所以FTD模型预测PD时效果稍好一点。
另外,将这些模型与已知的成熟生物标志物(如AD的血浆ptau217、PD的突触核蛋白聚集)比较,发现鉴别能力差不多(图7)。这很有意义,因为现在有针对tau蛋白、Aβ或突触核蛋白的新疗法,所以需要开发不依赖这些蛋白的新生物标志物。
总之,这些疾病特异性的生物标志物组合能较好地区分疾病与健康人,且它们在不同疾病间的预测效果差异,也反映了疾病之间分子层面的相似和不同程度。
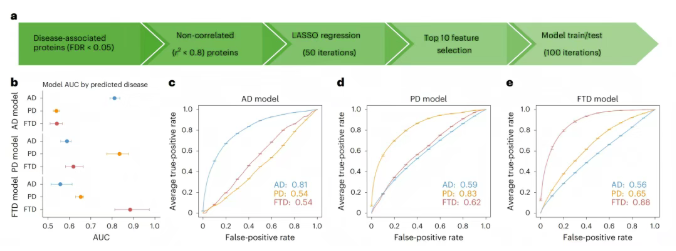
图6. AD、PD和FTD的疾病特异性预测模型
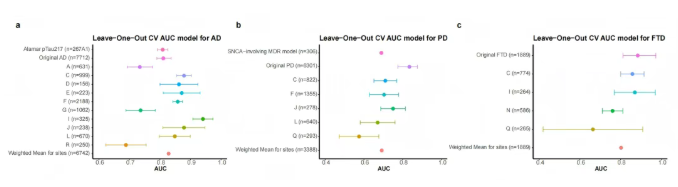
图7. AD、PD和FTD疾病特异性预测模型的留一站点交叉验证(CV)
研究结论
本文通过对阿尔茨海默病、帕金森病和额颞叶痴呆的血浆蛋白质组学分析,探究了三种神经退行性疾病的分子特征。研究发现,三者在蛋白质组学变化上存在一定重叠与差异,PD与FTD的蛋白质组学关联更紧密(r2=0.44),而AD与PD、AD与FTD的相关性较低(r2分别为0.04、0.07)。通路富集分析揭示了共同涉及的免疫、糖酵解及细胞外基质组织等通路,也识别出各疾病特异性通路,如AD的凋亡相关通路、PD的内质网-吞噬体通路、FTD的白细胞介素信号通路等。网络分析发现了AD中RPS27A、PD中IRAK4、FTD中MAPK1等关键调控蛋白。基于血浆的疾病特异性预测模型表现出较好的鉴别能力(AUC分别为 0.81、0.83、0.88),且具有疾病特异性,为这些疾病的诊断及新生物标志物开发提供了依据。
百趣生物血液蛋白冠-DIA 1X:以纳米材料表面修饰技术为核心支撑,通过纳米颗粒与血清/血浆样本的特异性共孵育反应,依托分子间特异性亲和力实现低丰度蛋白的高效富集,进而形成蛋白冠结构。该技术整合样本前处理自动化平台,耦合高灵敏度Astral质谱系统,采用数据非依赖采集(DIA)模式,可实现血液样本的深度蛋白质组学全景分析。相较于常规血液蛋白质组学检测方案,该技术的核心优势在于搭载自主研发的专利磁珠 D1(已获国家专利认证)。从磁珠的精密制备到标准化应用流程,均由专业设备与技术团队全程质控,确保磁珠批次间稳定性与均一性。基于此,检测数据呈现出卓越的质量特征:蛋白鉴定数量稳定突破5000+,蛋白稳定检出率达80%以上,同时显著提升功能性指标的检出丰度,为血液蛋白质组学研究提供了高维度、高可靠性的技术解决方案。