
文章标题:Multi-omics and network pharmacology reveal Huayu-Tongbi decoction reduced arthritis-related bone erosion
发表期刊:Chinese Medicine
影响因子:5.7
客户单位:广东省中医院
百趣提供服务:DIA中药入血组
研究背景
类风湿关节炎(Rheumatoid arthritis, RA)是一种常见的自身免疫性疾病,影响全球超过1%的人口,其主要特征为关节炎症和骨侵蚀,可导致患者活动能力下降和生活质量降低,且骨侵蚀会造成不可逆的关节损伤和功能障碍,而破骨细胞是这一过程的主要介导者。
目前用于治疗RA的药物如甲氨蝶呤(Methotrexate, MTX),虽有一定疗效,但无法有效针对骨侵蚀,还存在骨髓抑制等不良反应,因此开发能特异性靶向关节相关致病分子或细胞的新疗法十分关键。
临床研究表明,化瘀通痹汤(Huayu-Tongbi decoction, HT)作为RA的辅助治疗方法,能缓解相关症状,且可通过活化B细胞核因子κ轻链增强子(NF-κB)和Janus相关激酶/信号转导子和转录激活子(JAK/STAT)信号通路抑制成纤维细胞样滑膜细胞的炎症增殖。
然而,HT作为多靶点治疗药物的有效成分、作用机制,以及其对炎性关节炎中骨侵蚀的影响尚不明确。由于中药成分复杂,分析其药物成分并识别活性化合物是研究其疗效的必要环节,因此本研究采用网络药理学结合多组学的新兴策略,以探究HT的活性成分和靶点。
研究结果
1、HT减轻AIA大鼠的炎性关节炎
通过建立佐剂诱导关节炎(adjuvant-induced arthritis, AIA)大鼠模型(分为对照组、模型组、不同剂量HT组及MTX阳性对照组,干预30天),探究 HT对RA炎性症状的影响(图1A)。结果显示,AIA模型组大鼠体重增长减缓、关节肿胀明显、关节炎指数(Arthritis Index, AI)升高,血清炎症因子IL-6、破骨相关因子MMP-9和RANKL水平显著上升,踝关节滑膜组织出现增生及炎症浸润;而HT干预后,上述指标均呈剂量依赖性改善,其中高剂量HT组效果接近MTX组(图1B-H)。组织学结果显示,HT可减少滑膜增生和炎症细胞浸润(图1D-E)。这些结果证实HT能有效减轻AIA大鼠的炎性关节炎。
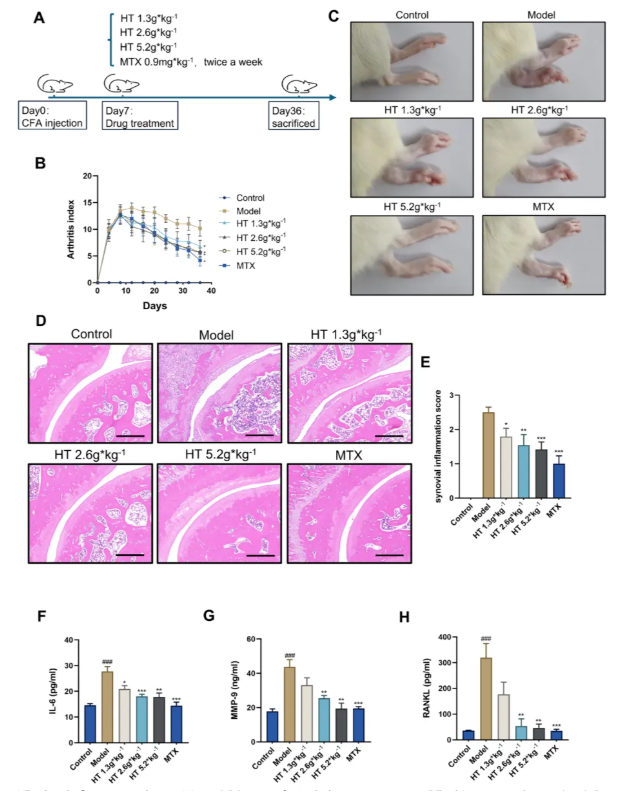
图1 HT减轻AIA大鼠的炎性关节炎
2、HT减轻AIA大鼠的软骨下骨破坏和关节软骨退变
通过对AIA大鼠踝关节进行组织染色及micro-CT扫描,探究HT对骨和软骨损伤的影响。结果显示,模型组大鼠踝关节出现明显软骨侵蚀、蛋白聚糖丢失(图2A-B),破骨细胞数量增加(TRAP阳性多核细胞增多,图2C-E),骨表面粗糙且结构破坏严重;HT干预后,软骨损伤评分降低,破骨细胞数量减少,骨结构破坏减轻,且高剂量HT组改善更显著(图2F)。两种检测均证实HT可减轻AIA大鼠软骨下骨破坏和关节软骨退变。
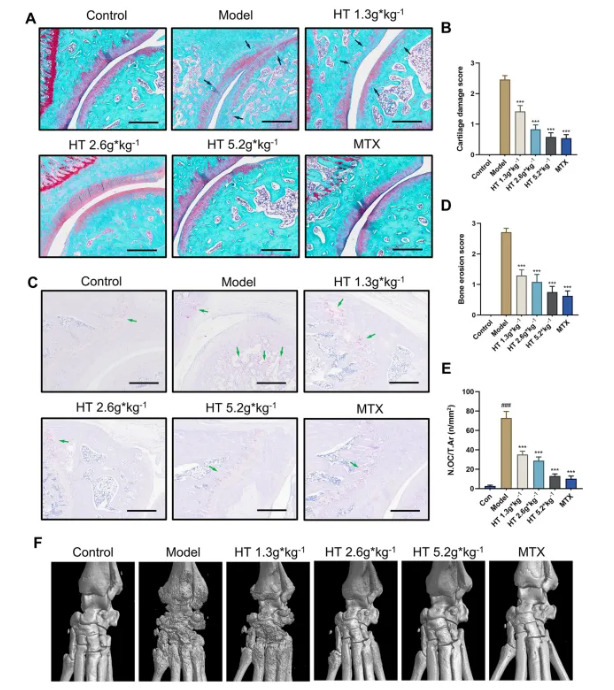
图2 HT减轻AIA大鼠的软骨下骨破坏和关节软骨退变
3、HT主要吸收成分的鉴定
为阐明HT缓解RA炎症及骨破坏的潜在作用机制,通过液相色谱-串联质谱对HT进行成分分析,并比较HT含药血清和空白大鼠血清检测结果,结果显示,与空白血清相比,HT含药血清中有110个入血物质(图3),其中44个为Level 1物质。
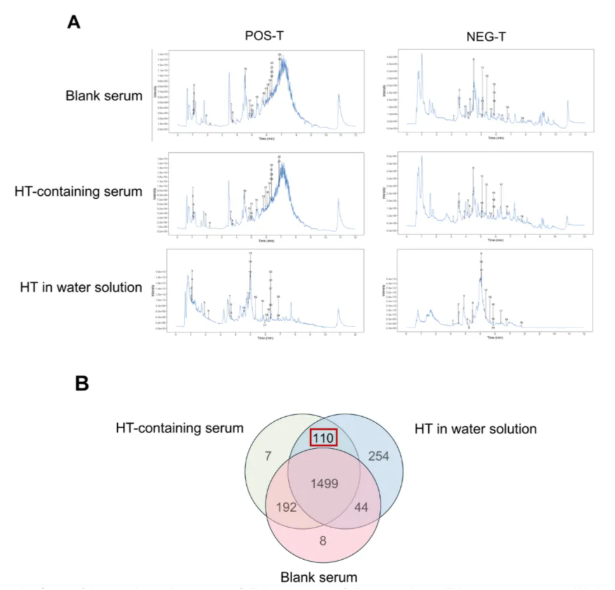
图3 HT主要吸收成分的鉴定
4、HT治疗RA主要靶点的网络药理学研究
通过网络药理学分析,探究HT治疗RA的关键靶点和通路。结果显示,RA差异基因与HT靶点交集得到89个核心靶点(图4B),PPI网络显示靶点间存在密切相互作用(图4C-D);GO富集分析表明HT治疗涉及炎症反应、骨代谢等生物学过程,KEGG富集于IL-17、NF-κB等与RA相关的通路(图4E-F)。这些结果揭示了HT多靶点作用的潜在机制。
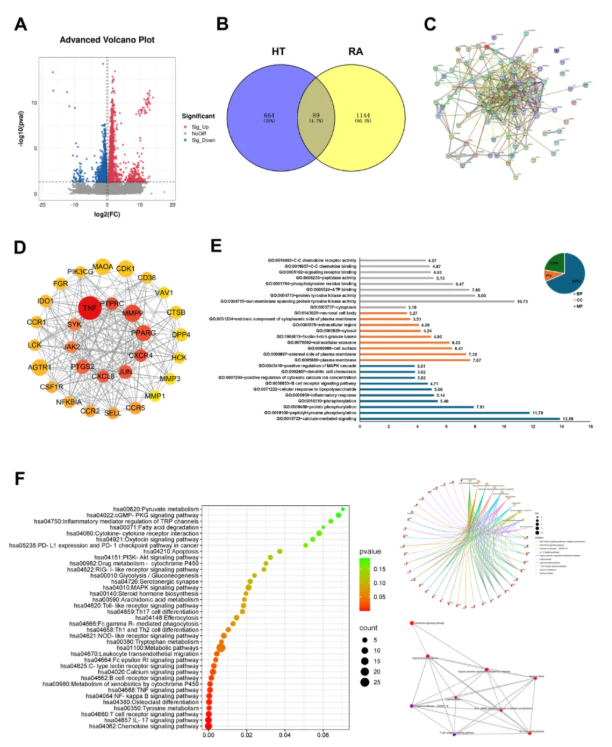
图4 HT治疗RA的主要靶点的网络药理学研究
5、 HT关键成分与靶点的分子对接
通过分子对接技术(PyMOL和Autodock Vina),分析HT关键成分与RA核心靶点的结合能力。结果显示,HT的活性成分(如丹酚酸A、4-甲氧基肉桂酸、7-羟基-2-(4-甲氧苯基)色烯-4-酮)与MMP9结合能分别为-9.2、-7.5、-10.1 kcal/mol,异黄腐酚等与PPARG结合能为-7.5~-7.8 kcal/mol(均<-5 kcal/mol,符合有效结合标准);三维交互图显示成分与靶点的稳定结合构象(图5)。这些结果验证了HT成分与靶点的特异性结合。
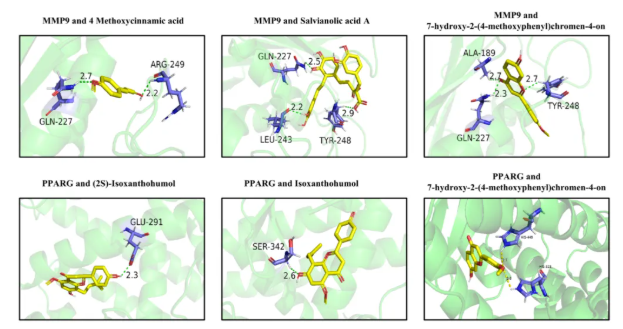
图5 三维图显示HT的关键组分与R中治疗靶点之间的分子对接相互作用
6、HT含药血清体外抑制RANKL诱导的破骨细胞分化
通过RAW264.7细胞建立RANKL诱导的破骨细胞分化模型,加入不同浓度HT含药血清,检测细胞活力及破骨细胞形成(图6)。结果显示,2.5%、5%、10% HT含药血清72小时内对细胞活力无显著影响(图6A),但可剂量依赖性减少TRAP阳性多核破骨细胞数量,其中10% HT组效果接近阳性药唑来膦酸。体外实验证实HT含药血清可抑制破骨细胞分化。
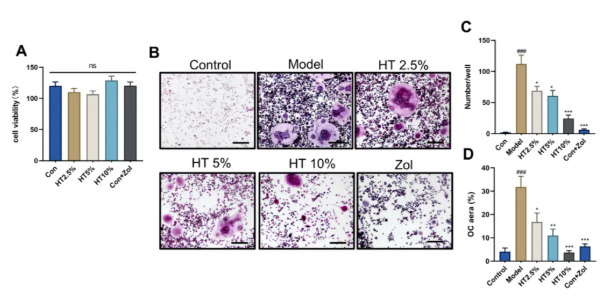
图6 HT含药血清体外抑制RANKL诱导的破骨细胞分化
7、RNA测序验证HT对破骨细胞分化的作用机制
为验证网络药理学结果并进一步探究HT干预的可能机制,通过RNA测序分析HT含药血清干预后的破骨细胞。结果显示,HT治疗能降低破骨分化相关基因的表达(如Tnf和Mmp-9等)(图7A-B);GO和KEGG分析表明这些基因富集于MAPK信号通路、PI3K/Akt信号通路及破骨细胞分化通路(图7C-D)。由此可看出,转录组学结果与网络药理学结果一致。
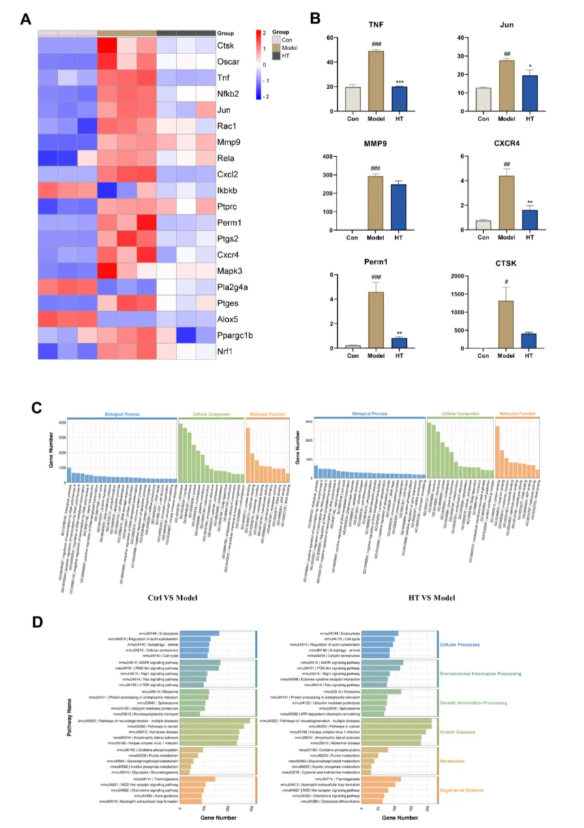
图7 RNA-seq验证HT影响破骨细胞分化的机制
8、代谢组学验证HT对破骨细胞分化的作用机制
破骨细胞分化过程中的代谢重编程在RA的骨降解过程中发挥重要作用,通过非靶向代谢组学分析HT含药血清干预后的破骨细胞,检测代谢物变化及相关通路。结果显示,模型组与对照组、HT组的代谢谱存在显著差异(图8A-E),且共鉴定62种差异代谢物(图8F);KEGG和GO富集分析表明,差异代谢物富集于花生四烯酸代谢、PPAR信号通路等通路(图8G),提示HT通过调节代谢过程影响破骨细胞功能,揭示了HT作用的可能代谢机制。
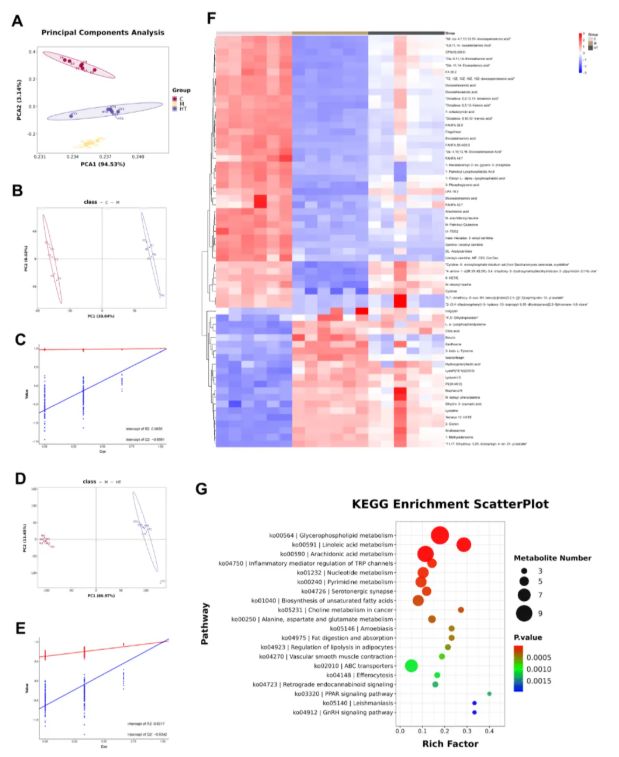
图8 采用代谢组学的方法验证HT在破骨细胞分化中的作用机制
9、多组学与网络药理学整合分析
通过整合代谢组学、转录组学数据与网络药理学结果,从多成分、多靶点、多效应角度探究HT减轻RA骨侵蚀的机制,分析三者共同涉及的通路及关键因子,并通过Western blot验证蛋白质水平。三者的交集分析及通路富集表明,花生四烯酸(AA)代谢、NF-κB通路、PPAR通路等生物学过程被显著富集(图9A);RNA-seq结果显示这些通路中的关键因子表达发生显著变化(图9B);Western blot进一步在蛋白水平证实,HT干预可影响PPAR通路(如PPAR-γ)、AA代谢(如COX-2)及NF-κB通路(如NF-κB2、Rel A)的关键蛋白表达(图9C)。这些结果共同揭示HT通过调控上述通路,改善RA伴随的破骨细胞诱导性骨侵蚀。
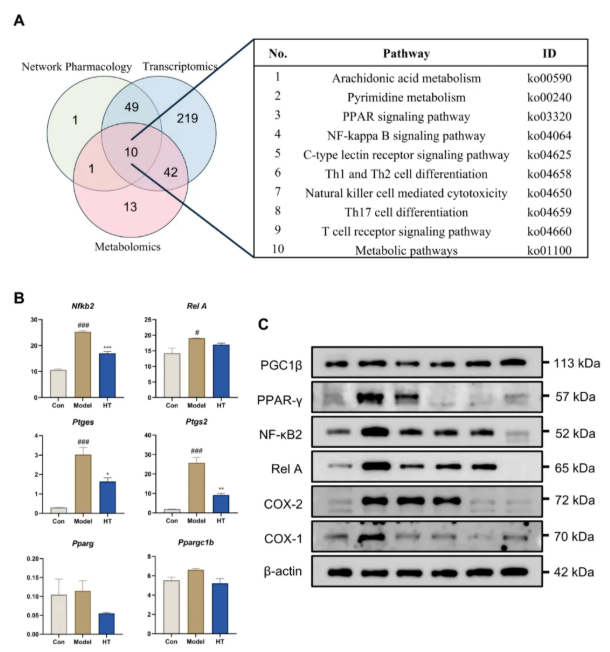
图9 整合代谢组学、转录组学和网络药理学分析
研究结论
本研究证实了HT对实验性关节炎的有益作用,并探讨了其具体机制,HT通过多靶点和多途径抑制骨细胞分化,减轻RA相关的骨侵蚀,为预防这一问题提供了潜在的治疗策略。
DIA中药入血组:百趣生物创新性地运用DIA数据采集模式采集血清中的中药药物成分,从数据采集上避免入血/入组织药物信息的遗漏,尽可能全面采集进入血液和组织的中药药物成分。并通过检索百趣生物自建中药标准品数据库和中药专属数据库,对血液样本或组织样本中的药效成分进行准确鉴定,同时结合药物成分在体内的代谢变化,并通过深入的分析内容呈现中药治疗疾病的作用机制。