
英文标题:In Situ Characterization and Deep Profiling of Engineered Multispecific Nanoparticle Metabolite Coronas for Precise Serum Diagnostics
中文标题:工程化多特异性纳米颗粒代谢冠原位表征与深度分析及其在精准血清诊断中的应用
发表期刊:Analytical Chemistry
影响因子:6.7
邓春晖教授担任百趣生物纳米磁珠技术首席科学家,长期聚焦纳米磁珠在组学领域的前沿研究与产业化应用。在长期深度协作与联合攻关下,继蛋白冠磁珠成功自主研发并应用后,双方再度携手推出代谢冠磁珠,实现“蛋白-代谢”双组学磁珠技术的协同突破。
该磁珠整合磁性纳米材料的高稳定性、高特异性与多靶点亲和设计优势,可高效捕获血清/血浆中的代谢物分子,显著提升低丰度代谢标志物的检出能力与覆盖度,为多组学联合分析与生物标志物发现提供了关键工具支撑。
研究背景
纳米医学领域中,工程纳米颗粒(NPs)凭借可定制的理化特性,在生物成像、靶向药物递送及精准诊断等方向展现出巨大应用潜力。然而,NPs进入生物体内接触血清、血液等生物流体后,其表面会自发吸附大量生物分子,形成稳定的生物分子冠,这一不受控的吸附行为会改变NPs的固有性质,进而影响其细胞摄取效率、生物分布及毒性,成为制约NPs临床转化的核心瓶颈。
生物分子冠由蛋白冠和代谢冠等共同构成。其中,蛋白冠的研究已形成成熟的理论体系与技术方法,而代谢冠作为冠结构的关键组成部分,虽具有远超蛋白质的丰度,且深度参与生物信号传导、与蛋白冠动态共存并相互作用,但其研究却长期处于滞后状态。这一现状的核心原因在于代谢物分子本身具有高度复杂性与多样性,且现有表征技术(如LC-MS、GC-MS、CE-MS等)均为异位分析方法,需通过离心、洗脱等步骤分离代谢冠,不可避免地造成冠结构破坏、样本损失及外源污染,无法还原其原生状态。
与此同时,子宫内膜异位症相关卵巢癌(EAOC)作为子宫内膜异位症恶性转化的罕见亚型,其早期诊断面临严峻挑战。EAOC早期症状与良性子宫内膜异位症高度重叠,传统超声诊断敏感性有限,而手术活检等有创手段易导致过度治疗,临床亟需无创、精准的早期诊断工具。
基质辅助激光解吸电离质谱(MALDI MS)凭借高灵敏度、高通量、抗干扰能力强等优势,为复杂生物流体代谢指纹分析提供了技术支撑。以Fe₃O₄为核心的磁性多功能纳米颗粒(MFNs)兼具表面可工程化、磁性快速分离及MALDI MS基质兼容三大特性,为代谢冠的原位表征提供了理想载体。基于此,本研究构建MFNs与MALDI MS整合的MMALDI MS高通量平台,实现代谢冠的原位形成与精准表征,结合XGB-SHAP算法解码代谢冠指纹,旨在填补代谢冠研究的方法学空白,同时为EAOC提供无创早期诊断方案,推动纳米医学向精准医疗落地。
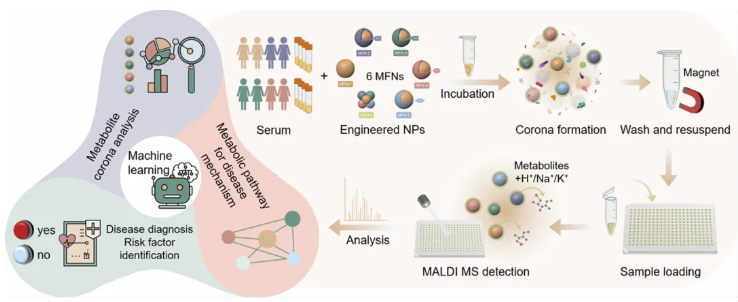
图文摘要
研究结果
1.MFNs的工程构建与表征
如工作流程示意图所示,研究团队将MALDI MS技术与MFNs多功能基质相结合,建立了用于代谢冠工程化形成与原位表征的统一平台。MFNs以Fe₃O₄为核心,通过五种差异化表面修饰策略精准设计系列产品(MFN-1~5):分别为无额外表面功能化的Fe₃O₄NPs(MFN-1)、硅涂层无封端核壳结构 Fe₃O₄NPs(MFN-2)、二氧化钛涂层核壳结构Fe₃O₄NPs(MFN-3)、氨基功能化Fe₃O₄NPs(MFN-4)及羧基功能化Fe₃O₄NPs(MFN-5)。
经透射电子显微镜(TEM)、动态光散射(DLS)、X射线光电子能谱(XPS)及Zeta电位表征验证,五种MFNs均呈现规整球形核壳结构(图S1),表面特性与设计方案精准匹配。
该MFNs兼具三大关键功能:表面可工程化特性支持代谢冠定向形成,约15秒快速磁性分离可最大程度避免冠结构破坏,MALDI MS基质兼容性允许无需洗脱直接原位检测,成功解决传统异位方法分离过程中冠结构破坏、样本损失的核心痛点。同时,五种MFNs在形态、电荷、表面基团等理化性质上的明确差异,为后续实现代谢物特异性吸附、拓展血清代谢组覆盖度提供了关键前提。
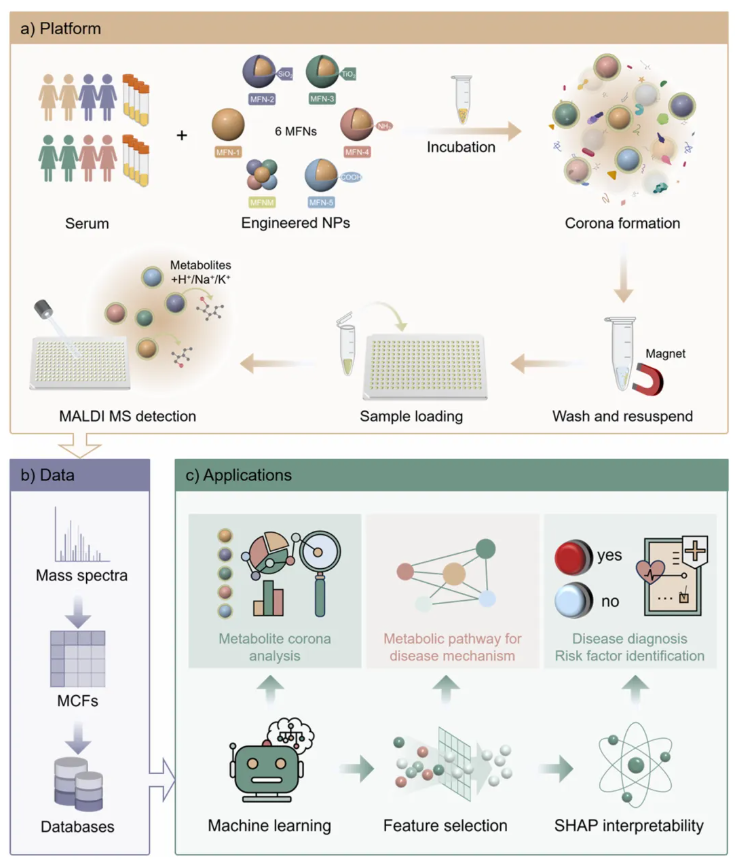
工作流程示意图:(a)平台开发;(b)数据库构建;(c)技术应用

图S1.透射电镜图
2.MFN特异性代谢冠的形成
工作流程示意图所建平台在方法学上优势显著:单样本代谢冠分析(除孵育外)仅需2-3分钟,效率较传统超离心法提升10倍以上;无需繁琐去蛋白质步骤即可直接分析血清样本,最大程度保留原始纳米生物界面特征,具备卓越抗蛋白干扰能力。
代谢组学应用评价显示,五种表面理化性质差异化的MFNs从100-1000Da分子量范围的原始质谱中提取出292个代谢物特征(图1a),构建出各自独特的代谢冠指纹图谱(MCFs)。不同MFN的代谢冠在分子量分布(图1b)、聚类相似度(图1c)上差异显著,证实表面理化性质是代谢冠组成的关键调控因素。经稀疏偏最小二乘判别分析(sPLS-DA)和随机森林(RF)算法筛选,结合HMDB数据库匹配与LC-MS验证,总计23个差异代谢物特征被鉴定(图1d),可100%区分不同MFN的代谢物吸附模式(AUC=1.00),构成其表面吸附模式的 “分子身份证”。
进一步解码吸附机制发现,表面工程赋予MFNs特异性分子作用力优势,血清代谢物的选择性吸附由弱分子间相互作用(静电力、氢键、亲疏水性)与强相互作用(配位效应)共同主导。不同表面修饰的MFN存在明确吸附偏好:如氨基功能化的MFN-4偏好吸附负电或电负性代谢物,羧基功能化的MFN-5在静电屏蔽条件下偏好长链疏水代谢物,为精准调控代谢冠形成提供了理论依据。
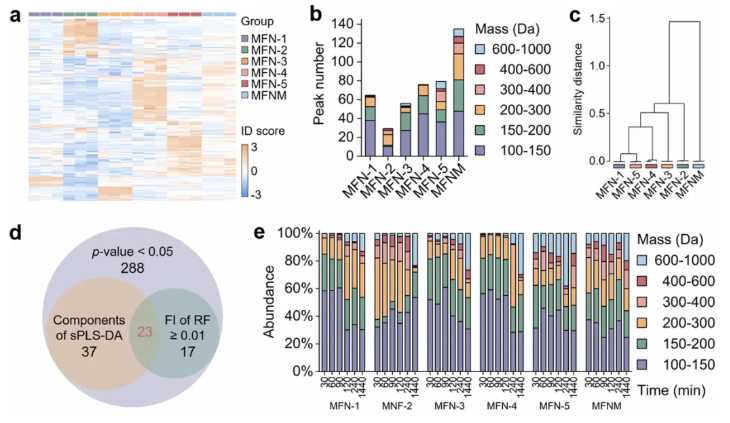
图1.MFN特异性代谢冠的代谢组学表征
3.MFN结合代谢冠的时间动态
生物分子在纳米颗粒表面的吸附是一个动态过程,影响因素相互作用复杂。尽管蛋白质结合动力学可通过Vroman效应(生物流体中,蛋白质在材料表面的吸附存在竞争性置换现象:低亲和力蛋白质先快速吸附至表面,随后逐渐被高亲和力蛋白质取代,最终形成稳定的蛋白质吸附层)解释,但代谢物等其他生物分子的冠结合动力学仍缺乏实验支撑。为探究代谢冠的时间动态特征,研究纳入6个关键时间点(30、60、90、120、240、1440分钟),系统追踪 “MFNs-代谢冠” 的动态演变。
结果显示,所有MFNs形成的代谢冠中,<300Da小分子代谢物始终占主导,且随血清暴露时间延长,代谢物组成按分子量呈现明显重构(图1e),中晚期变化最为显著。聚类分析验证了时间特异性:无监督层次聚类与基于900个MCFs样本的K-means聚类(图2a-e),均能100%准确按时间点区分MCFs,证实代谢冠的时间动态特征具有高度可重复性。此外,不同表面功能化MFNs形成的代谢冠均展现独特时间动态轨迹,进一步印证表面理化性质与时间因素对代谢冠形成的共同调控作用。综上,代谢物暴露时间是影响代谢冠组成与演变的关键因素。
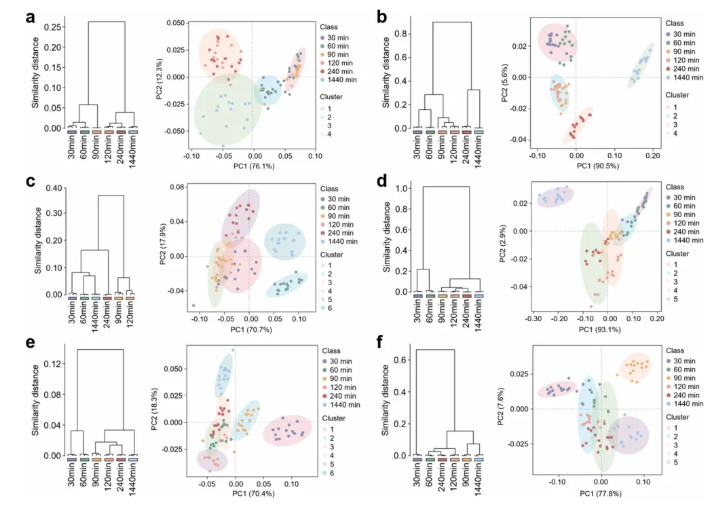
图2.血清暴露时间对MFN结合的代谢冠的影响
4.五种MFN组合实现血清代谢组深度覆盖
由于不同表面理化性质的MFN均能捕获血清代谢组,且各自具有独特的MCFs,联合使用可显著提升检测覆盖度。对此,研究团队将五种差异化修饰的MFN按等质量比混合,成功制备兼具多重吸附特异性的MFNM。其代谢物结合图谱与单一MFN既有重叠又存在显著差异(图1a-c、e,图2f):与单一MFN相比,捕获的血清代谢物数量提升1.71-4.66倍(图1b);较标准MALDI MS方案,直接血清代谢物检测覆盖度飙升135%-150%,实现血清代谢组深度解析。在此基础上,研究团队又以MFNM为多功能基质,开发出MFNM辅助激光解吸电离质谱(MMALDI MS)平台,可从复杂生物流体中高覆盖、可重复且稳定获取MCFs,为后续临床样本数据库构建及疾病诊断应用提供了核心技术支撑。
5.MMALDI MS应用:子宫内膜异位症恶性转化的无创早期诊断工具
子宫内膜异位症作为常见的良性慢性妇科疾病,约0.14%-2.90%的患者可能恶变为EAOC(一种罕见的卵巢恶性肿瘤亚型)。目前EAOC发病机制尚未明确,缺乏特异性诊断标准,导致早期诊断困难,且尚无成熟的非侵入性检测方法,临床需求迫切。
为破解这一难题,研究团队收集192例确诊患者血清样本,分为M-OC组(EAOC患者,97例)和B-OC组(良性子宫内膜异位囊肿患者,95例),利用MMALDI MS平台构建了包含393个代谢特征的MCF数据库。然而,常规主成分分析(PCA)的无监督聚类未能实现两组样本的有效分离,表明需要借助更复杂的机器学习算法提升分类效率。
对比RF、SVM、LR和XGB四种算法(图3a),结果显示,XGB模型综合性能最优,是区分两组样本的最有效分类算法(图3b)。经贝叶斯优化结合10折交叉验证调参后,该诊断分类器在训练集和测试集中的AUC分别达到0.96和0.99(图3c),且校准曲线显示预测结果与实际情况高度吻合(图3d),成功实现对EAOC患者与良性对照的精准区分。
尽管XGB算法预测性能优异,但其 “黑箱” 特性会掩盖内部决策过程,影响临床应用可信度。为提升模型可解释性,团队整合SHAP分析构建了XGB-SHAP模型(图3e)。其中,SHAP值越高代表恶性风险越高,通过SHAP汇总图可直观呈现特征重要性与贡献模式。基于SHAP排序法(图3f)、XGB特征评分(图3g)及新增的 “排名评分法”,研究确定了5个特征为组合优化经验阈值(图3h),在保持分类器最优准确率的同时,筛选出8种核心生物标志物,仅用8个特征便可实现高精准区分,降维效能突出。
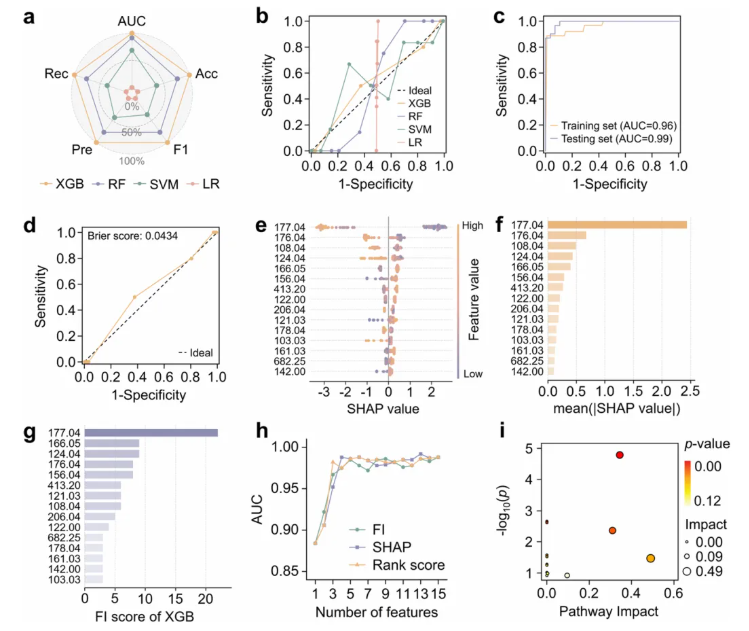
图3.基于MMALDI MS平台的子宫内膜异位症恶性转化早期诊断模型构建与特征筛选
进一步分析发现,8种核心差异代谢物主要富集于三条关键代谢通路(图3i):维生素B6代谢、组氨酸代谢、丙氨酸/天冬氨酸/谷氨酸代谢。通过SHAP力图(图4a-b)和依赖图(图4c),高风险恶变的代谢特征被解析(3种代谢物上调、5种代谢物下调)。这些结果不仅为EAOC发病机制提供了新的代谢视角,更明确了驱动良恶性判断的关键代谢物变化,为临床决策提供直观依据。
综上,研究团队将MMALDI MS平台与可解释机器学习(XGB-SHAP)深度融合,开发出一套完整方案,为子宫内膜异位症恶性转化的无创、早期、精准诊断提供了强大的新工具与新见解,有望破解EAOC临床诊断困境。
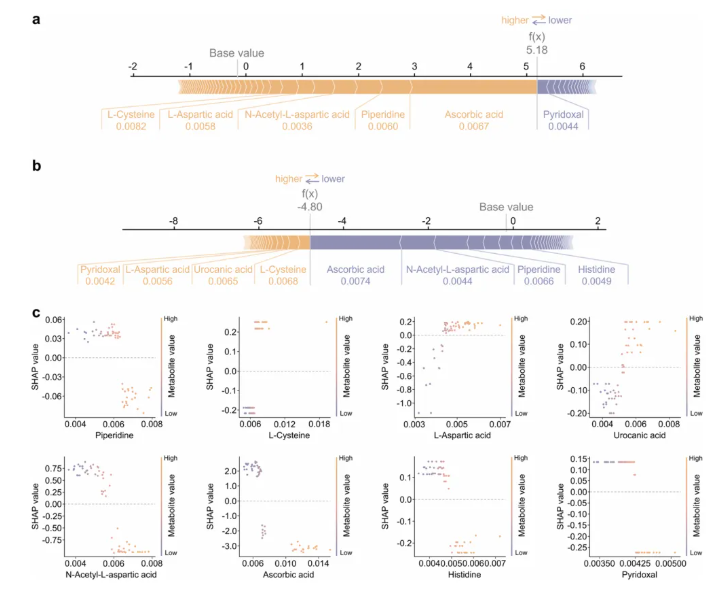
图4.基于XGB-SHAP模型的子宫内膜异位症恶性转化可解释性分析
研究结论
本研究针对代谢冠表征难、易受干扰、研究滞后的核心问题,开发以Fe₃O₄为核心的5种表面修饰差异化MFNs,构建MMALDI MS高通量平台,实现蛋白质共存下MCFs的原位、快速、高覆盖捕获,证实了NPs表面理化性质与代谢物暴露时间是其形成与演变的关键调控因素。此外,结合XGB-SHAP算法,从192例临床血清样本中筛选出8种经验证的核心生物标志物,成功构建EAOC无创早期诊断模型,并揭示3条相关代谢通路。该研究既建立可规模化的代谢冠研究框架,又为疾病精准诊断提供突破性工具,拓展了纳米医学在精准医疗的应用场景。
代谢冠磁珠的成功推出,是百趣生物与邓春晖教授团队合作进程中的重要里程碑。未来,双方将继续深化合作,推动该磁珠在疾病诊断、标志物筛选等领域的应用,并通过优化现有技术,探索磁珠在新兴组学领域的应用可能,助力相关科研成果转化,为组学研究发展注入动力。