
文章标题:Targeting polyamine metabolism and ferroptosis enhances the efficacy of KRAS-targeted therapy depending on KEAP1 status
发表期刊:nature communications
影响因子:15.7
客户单位:复旦大学附属中山医院
百趣提供服务:新一代代谢组学NGM 2 Pro
研究背景
KRAS突变在胰腺癌、结直肠癌、肺癌等癌症中高发,虽索托拉西布等KRAS靶向抑制剂已实现临床突破,但疗效常因KEAP1、LKB1等共突变显著受限。铁死亡作为一种铁依赖、以多不饱和脂肪酸过氧化为特征的细胞死亡方式,已被证实可有效克服肿瘤治疗耐药性,且KRAS突变对脂质代谢和抗氧化反应的复杂调控,为通过促进铁死亡增强KRAS靶向治疗效果提供了潜在可能,不过KEAP1突变会破坏KEAP1-NRF2抗氧化通路,可能影响铁死亡诱导效果。多胺(精胺、亚精胺等)在肿瘤细胞持续增殖中起关键作用,其分解代谢关键酶SAT1可通过催化多胺乙酰化、经PAOX氧化生成ROS进而促进铁死亡,KRAS突变肿瘤细胞常依赖高多胺水平维持增殖,靶向SAT1介导的多胺代谢已成为癌症治疗潜在方向,但该方向在KRAS靶向治疗中的应用及KEAP1状态对其的调控作用尚未得到充分研究,因此本研究旨在通过相关实验探究基于KEAP1状态的多胺代谢与铁死亡在KRAS靶向治疗中的作用及机制,为KRAS突变癌症的精准治疗提供理论支持。
研究结论
01.多胺以KEAP1依赖方式协同增强KRAS抑制剂的疗效
通过889种代谢物库筛选(图1A),发现精氨酸、鸟氨酸、亚精胺、精胺等多胺类代谢物能显著增强KRAS抑制剂(索托拉西布、阿达格拉西布)对MIAPACA2细胞的抑制作用(图1B)。在15种KRASG12C突变细胞系中,10种细胞表现出协同效应,5种无协同效应(图1D),结合CCLE数据库分析发现,多胺仅在 KRASMU/KEAP1WT细胞系(如MIAPACA2、H1373)中增强KRAS抑制剂敏感性,在KRASMU/KEAP1MU细胞系(如H23、H2122)中无此作用(图1E),且该结果在新型KRAS抑制剂(fulzerasib、garsoasib)、泛KRAS抑制剂(BI-2493)和KRASG12D抑制剂(MRTX1133)中均得到验证。在PAAD和LUAD患者来源类器官(patient-derived organoids, PDOs)中(图1F-G),亚精胺能显著增强KRAS抑制剂对 KRASMU/KEAP1WT PDOs的抑制作用(图1H-I),但对KRASMU/KEAP1MU PDOs无影响(图1J-K)。功能验证显示,敲除MIAPACA2和H1373细胞的KEAP1后,多胺的协同作用消失;在H23细胞中过表达KEAP1,则恢复多胺对KRAS抑制剂的敏感性(图2A),证实KEAP1状态是多胺发挥协同作用的关键。
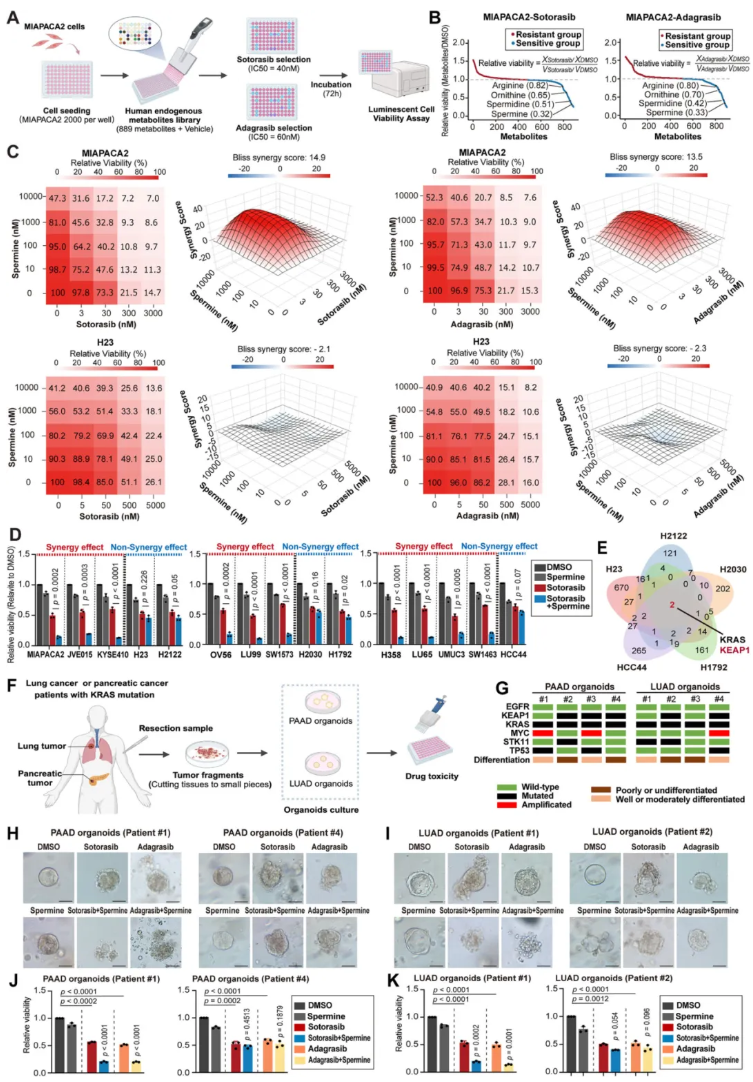
图1. 多胺以KEAP1依赖的方式协同增强KRAS抑制剂的疗效
02.KEAP1WT依赖的SAT1上调增强多胺与KRAS抑制剂的协同作用
RNA-seq分析显示,KRAS抑制剂处理后,KRASMU/KEAP1WT的MIAPACA2和H1373细胞中SAT1(多胺分解代谢关键酶)显著上调,而 KRASMU/KEAP1MU的H23细胞中SAT1显著下调,多胺合成关键酶ODC1在两组细胞中均下调(图2C-D)。代谢组学检测发现,KRAS抑制剂处理后,MIAPACA2和H23细胞中精胺、亚精胺及其乙酰化产物(N¹-乙酰精胺、N¹-乙酰亚精胺)水平降低,且H23细胞中乙酰化产物的降低更为显著(图2E)。SAT1-KO的MIAPACA2细胞中,多胺无法增强KRAS抑制剂的疗效;而SAT1-OE的H23细胞中,多胺显著提升药物敏感性,但酶活性位点突变的SAT1-Y140F无此作用(图2G),证实SAT1的酶活性是协同作用的核心。进一步研究显示,敲除KEAP1可抑制KRAS抑制剂诱导的SAT1上调,过表达KEAP1则可逆转H23细胞中SAT1的下调(图2H),且KEAP1突变体同样能上调SAT1表达,表明KEAP1对SAT1存在负向调控,且该调控在KRAS抑制剂处理后发生逆转。
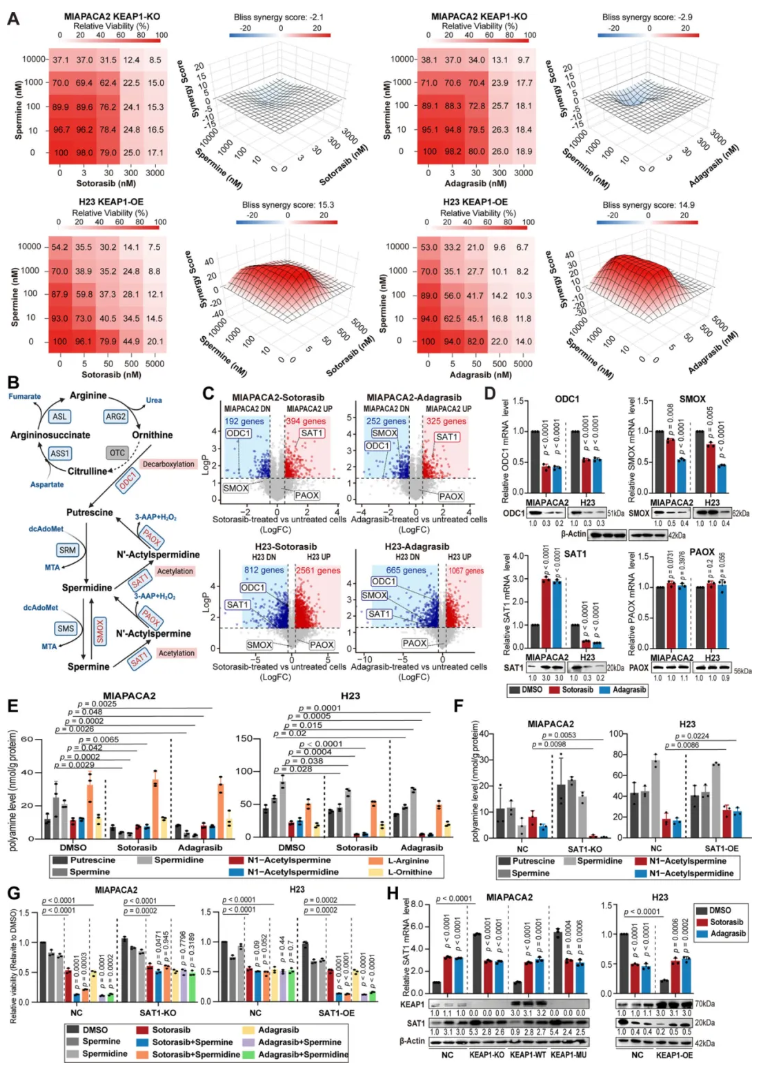
图2. KEAP1WT依赖的SAT1上调增强了多胺与KRAS抑制剂之间的协同作用
03.SAT1介导的多胺分解代谢通过铁死亡增强KRAS 抑制效果
在MIAPACA2细胞中,多胺与KRAS抑制剂联合处理后,铁死亡标志物MDA含量(图3B)、脂质过氧化水平(图3C)、细胞内亚铁离子浓度(图3D)显著升高,透射电镜观察到线粒体皱缩、嵴消失(图3E-F),而铁死亡抑制剂(Fer-1、DFO)可完全阻断多胺与KRAS抑制剂的协同作用,凋亡或坏死抑制剂无此效果(图3A)。SAT1-KO的MIAPACA2细胞中,联合处理未引起铁死亡标志物的显著变化;而SAT1-OE的H23细胞中,铁死亡标志物显著升高,线粒体损伤加重,但SAT1-Y140F突变体无法诱导该效应(图3H-L)。此外,多胺的补充可增加细胞内H₂O₂生成,该效应可被SAT1-KO或PAOX-KO阻断,证实SAT1介导的多胺N1-乙酰化与PAOX介导的乙酰化多胺氧化反应共同产生H₂O₂,通过芬顿反应促进铁死亡,进而增强KRAS抑制剂的细胞毒性。
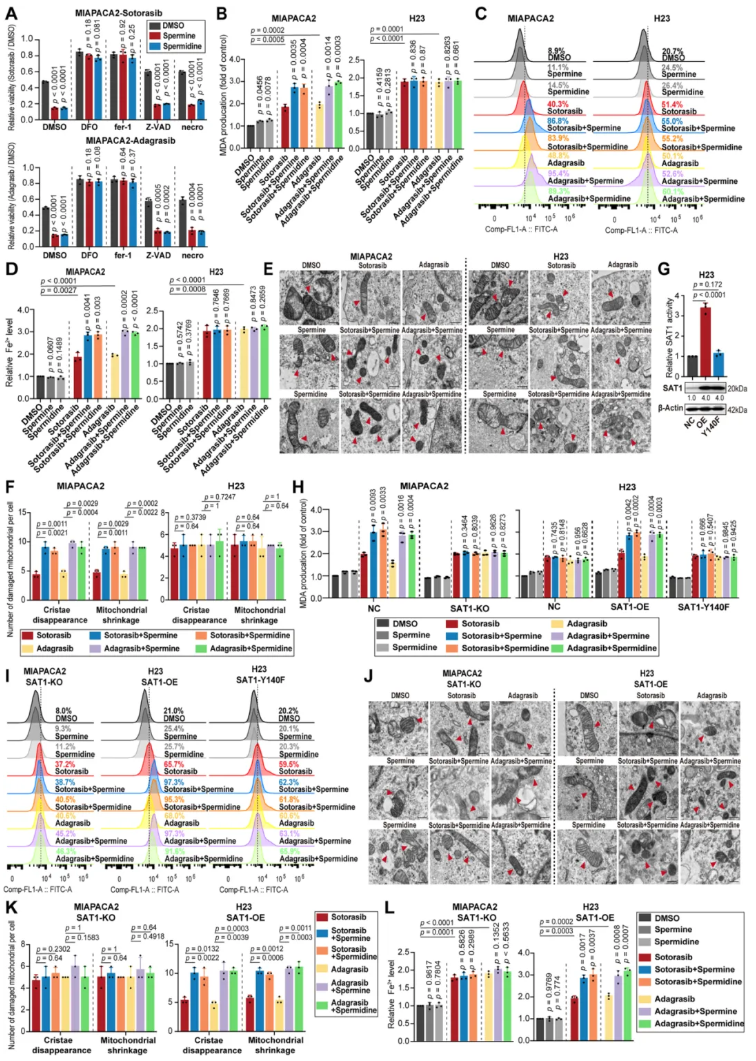
图3. SAT1介导的多胺分解通过铁死亡增强KRASMU/KEAP1WT中的KRAS抑制效果
04.通过SAT1介导的多胺代谢与铁死亡克服药物耐药性
通过7个月梯度递增KRAS抑制剂浓度,成功构建MIAPACA2和H23的耐药细胞系(IC₅₀较亲本细胞升高10倍以上)(图4A-B)。在MIAPACA2耐药细胞(KRASMU/KEAP1WT)中,多胺仍能显著增强KRAS抑制剂的疗效;但在H23耐药细胞(KRASMU/KEAP1MU)中无协同作用(图4C)。RNA-seq和WB结果显示,耐药的MIAPACA2细胞中SAT1仍保持高表达,而耐药的H23细胞中SAT1表达进一步下调(图4E-F)。代谢组学分析发现,耐药细胞中精胺、亚精胺水平降低(与多胺合成关键酶ODC1下调一致),且H23耐药细胞中N¹-乙酰精胺和N¹-乙酰亚精胺的降低更为显著(图4G)。联合处理后,MIAPACA2耐药细胞的脂质过氧化水平显著升高(图4H),证实SAT1介导的多胺代谢与铁死亡通路可有效克服KRAS靶向治疗的耐药性。
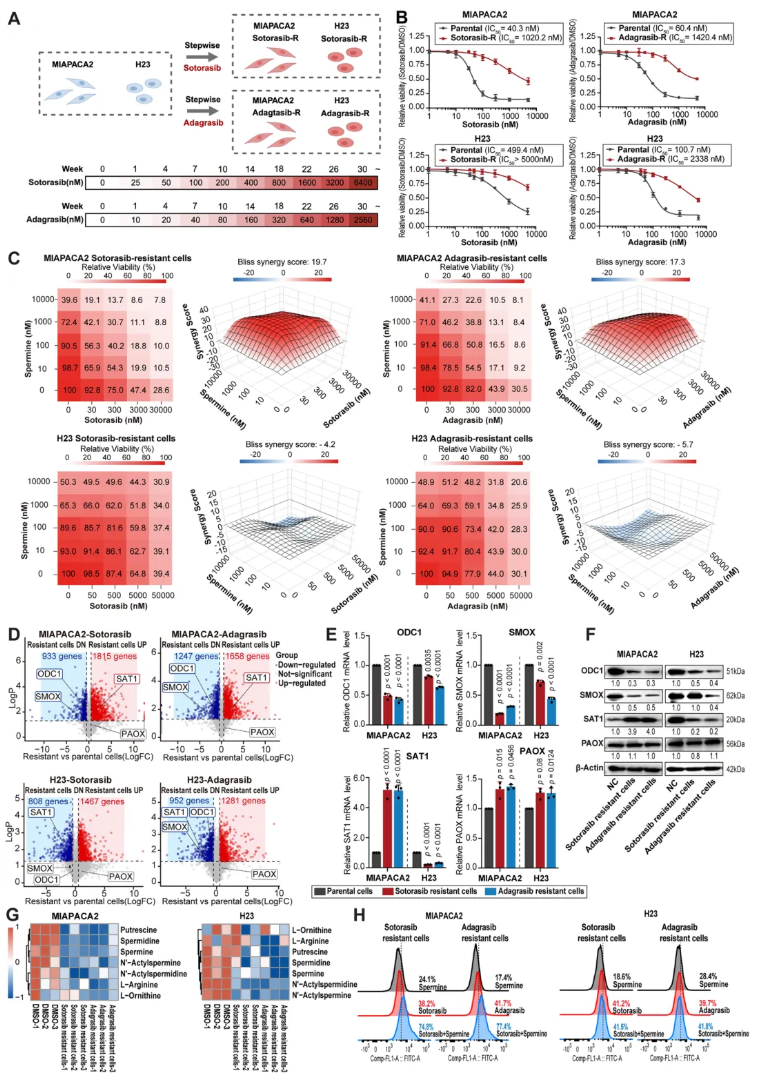
图4. 通过SAT1介导的多胺代谢和铁死亡克服药物耐药性
05.KRAS抑制剂通过JNK/NRF2/SAT1和JNK/c-Jun/SAT1通路调控SAT1表达
WB分析显示,KRAS抑制剂处理后,H23细胞(KRASMU/KEAP1MU)中NRF2表达与SAT1同步下调,且磷酸化JNK(p-JNK)和磷酸化c-Jun(p-c-Jun)在MIAPACA2和H23细胞中均显著上调(图5A)。JNK抑制剂(JNK-IN-8、JNK-IN-11)可逆转MIAPACA2细胞中SAT1的上调,同时阻止H23细胞中NRF2的降解和后续SAT1的下调,而NF-κB抑制剂无此效果(图5B)。ChIP-qPCR和DNA pull-down实验证实,NRF2和c-Jun均能结合到SAT1的启动子区域(图5C-D);双荧光素酶报告基因实验显示,KRAS抑制剂可增强MIAPACA2细胞中SAT1的转录活性(依赖c-Jun结合位点),抑制H23细胞中SAT1的转录活性(依赖NRF2结合位点)(图5F)。免疫荧光染色进一步验证,MIAPACA2细胞中KRAS抑制剂促进c-Jun与SAT1启动子结合,而H23细胞中则促进NRF2降解,进而抑制SAT1表达(图5G-H),表明KRAS抑制剂根据 KEAP1 状态,通过JNK/c-Jun/SAT1(KEAP1WT)或JNK/NRF2/SAT1(KEAP1MU)双通路特异性调控SAT1转录。
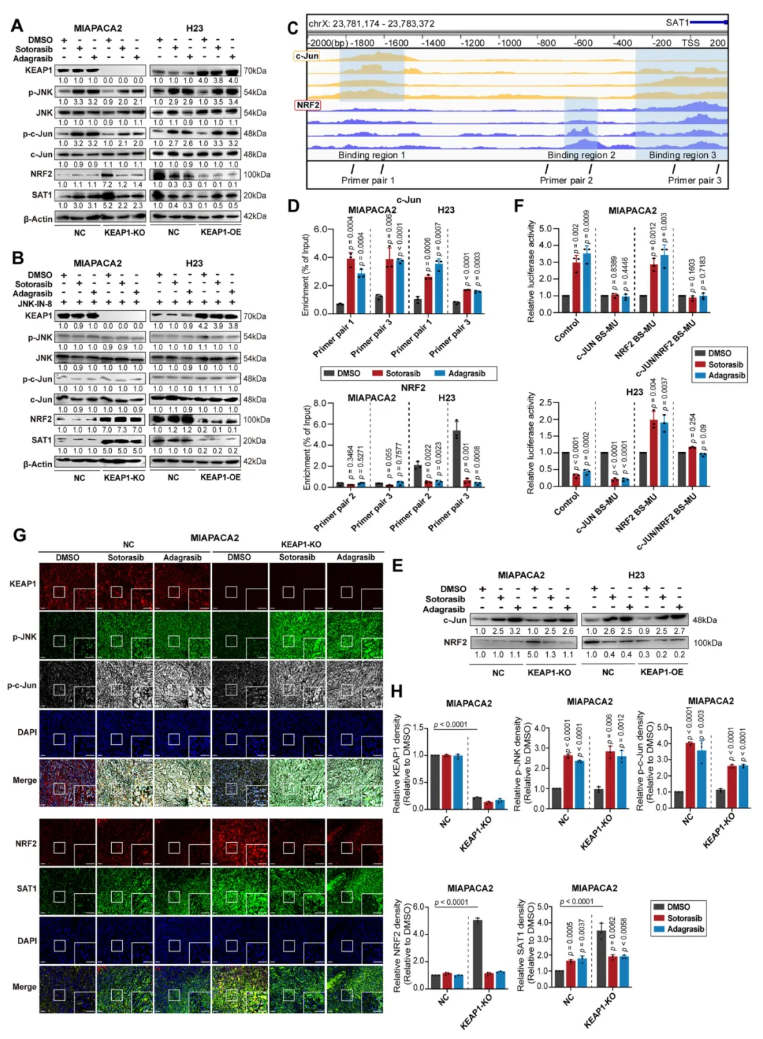
图5. KRAS抑制剂通过JNK/NRF2/SAT1和JNK/c-Jun/SAT1通路调节SAT1表达
06.靶向SAT1介导的多胺代谢在体内模型中增强KRAS抑制剂的疗效
在KRASMU/KEAP1WT的PAAD和LUAD PDOs中,多胺的补充可增加MDA含量,增强KRAS抑制剂的疗效,该效应被SAT1-KO阻断;在KRASMU/KEAP1MU的PAAD和LUAD PDOs中,仅当SAT1-OE时,多胺才能显著提升药物敏感性(图6C-D)。异种移植模型中,MIAPACA2细胞移植裸鼠经精胺与索托拉西布联合治疗后,肿瘤体积和重量显著小于药物单药组(图6F-H);H23细胞移植裸鼠经AAV介导SAT1过表达后,联合治疗显著抑制肿瘤生长(图6I-K)。在KRASG12C突变自发性肺癌小鼠模型中(图6L),联合治疗组的肿瘤经CT扫描显示几乎完全消失,小鼠生存期显著延长(图6M-N),证实靶向SAT1介导的多胺代谢在体内可有效增强KRAS靶向治疗的疗效。
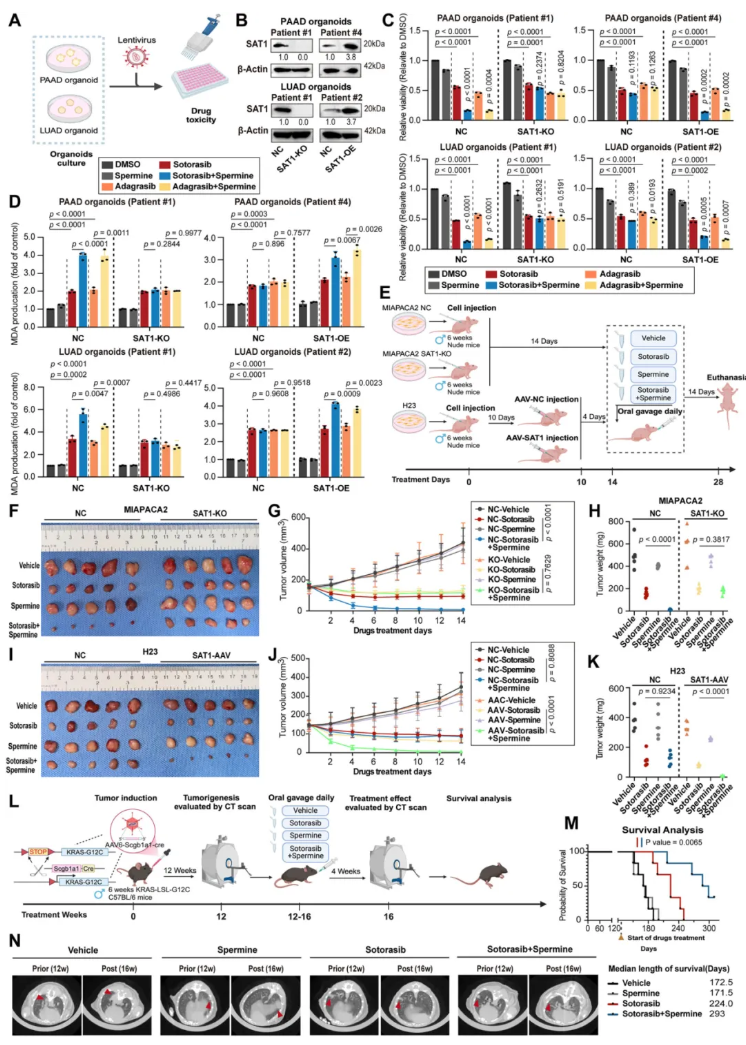
图6. 精确靶向SAT1介导的多胺代谢以增强PDOs、异种移植和自发性肺癌小鼠模型中的KRAS抑制剂效果
研究总结
本研究通过代谢物库筛选、细胞实验、体内模型验证及机制探究,明确多胺可通过SAT1介导的多胺分解代谢促进铁死亡,进而增强KRAS靶向治疗的疗效,且该效应依赖KEAP1状态。具体机制为:在KRASMU/KEAP1WT肿瘤中,KRAS抑制剂激活JNK/c-Jun通路,促进SAT1转录;多胺补充后,SAT1催化精胺、亚精胺乙酰化,经PAOX氧化生成H₂O₂,通过芬顿反应诱导铁死亡,增强药物敏感性;在KRASMU/KEAP1MU肿瘤中,KRAS抑制剂激活的JNK通路促进NRF2降解,导致SAT1表达下调,需先通过慢病毒或AAV介导SAT1过表达,多胺才能发挥铁死亡诱导和药物增敏作用。该研究还证实,靶向SAT1介导的多胺代谢可有效克服KRAS靶向治疗的耐药性,在患者来源类器官、异种移植模型和自发性肺癌小鼠模型中均展现出显著的治疗效果。综上,本研究揭示了KEAP1状态对多胺代谢与KRAS靶向治疗协同作用的调控机制,提出以SAT1为核心的精准治疗策略,为KRAS突变癌症(尤其是伴KEAP1共突变的患者)提供了新的治疗方向和实验依据。
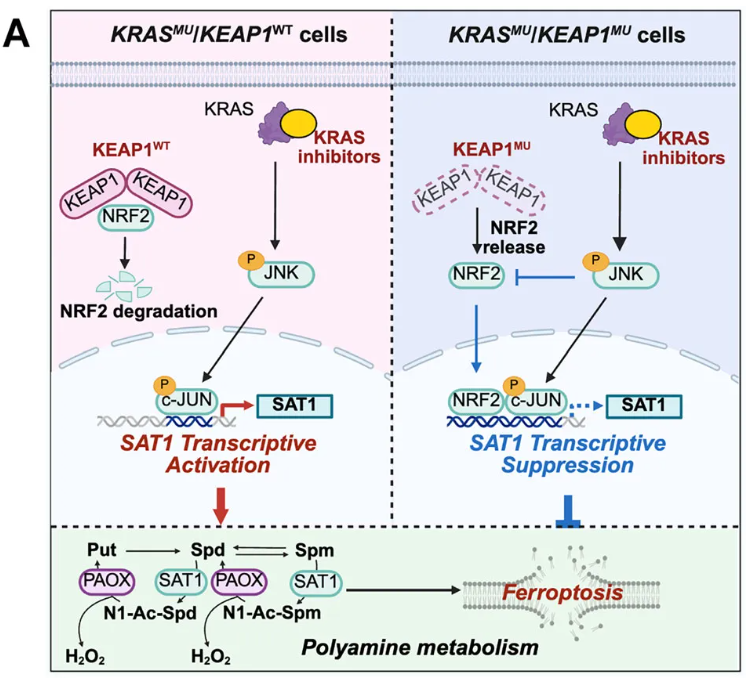
图7. 针对SAT1介导的多胺代谢和铁死亡,以增强不同KEAP1状态下KRAS突变癌症的靶向治疗效果