
文章标题:FoxO1/PINK1/Parkin-dependent mitophagy mediates the chondroprotective effect of Guzhi Zengsheng Zhitong decoction in osteoarthritis
发表期刊:Phytomedicine
影响因子:8.3
客户单位:山西医科大学
百趣提供服务:DIA中药入血组
研究背景
骨关节炎(Osteoarthritis, OA)是骨科领域的重大挑战,随人口老龄化对生活质量的影响和医疗经济负担日益显著,软骨细胞功能障碍是疾病进展的核心环节。FoxO1转录因子可通过介导线粒体自噬维持软骨细胞稳态,是OA治疗的潜在靶点,而针对FoxO1-线粒体自噬轴的中药相关研究仍较为有限。国医大师刘柏龄基于“补肾壮骨”理论研发的骨质增生止痛汤(Guzhi Zengsheng Zhitong Decoction, GZZD),临床治疗OA疗效显著、不良反应低,前期研究证实其可调节软骨细胞增殖分化、平衡骨代谢,但对线粒体稳态调控的具体机制尚未明确。本研究通过多组学整合分析结合分子生物学技术,阐释GZZD通过FoxO1调控线粒体自噬保护软骨细胞的作用机制并鉴定其活性成分,为OA的FoxO1靶向治疗及传统中药理论的现代化阐释提供科学依据。
研究结论
01.GZZD减轻MIA诱导的大鼠骨性关节炎
如图1A所示,作者通过膝关节腔内注射碘乙酸钠(MIA)建立了大鼠OA模型。注射后,OA组大鼠股骨头软骨显著增生,股骨髁损伤严重,滑膜明显红斑、增厚,关节组织呈淡黄色改变,与既往报道一致,提示造模成功。与OA组相比,口服硫酸葡萄糖胺(Glucosamine sulfate, GS)或GZZD均能显著改善软骨增生,减轻股骨髁红斑,抑制OA样病变。
H&E、甲苯胺蓝及番红固绿染色显示,OA大鼠出现软骨变薄、表面缺损、骨小梁坏死及纤维组织增生(图1B)。GS及高、低剂量GZZD均显著缓解上述病理改变。依据番红固绿染色计算的OARSI评分,OA组显著升高,提示软骨损伤重、进展快(图1C);给药后评分极显著下降,表明疾病进展减缓。
ELISA检测血清IL-1β、IL-6、TNF-α(图1D-F)发现,OA大鼠三种炎症因子显著升高,提示炎症反应强烈;GZZD治疗后其浓度显著下降,显示GZZD在OA进程中具有显著抗炎作用。
Micro-CT(图1G)显示,OA诱导后股骨髁软骨下骨被严重侵蚀,骨组织破坏广泛;GZZD有效保护骨组织免受进一步损伤,且能部分恢复骨量。骨体积分数(BV/TV)是骨量关键指标,OA组显著降低,GZZD可使其部分恢复;骨表面积及结构模型指数(SMI)亦在OA模型中显著下降,经GZZD给药后得到改善(图1H-J)。
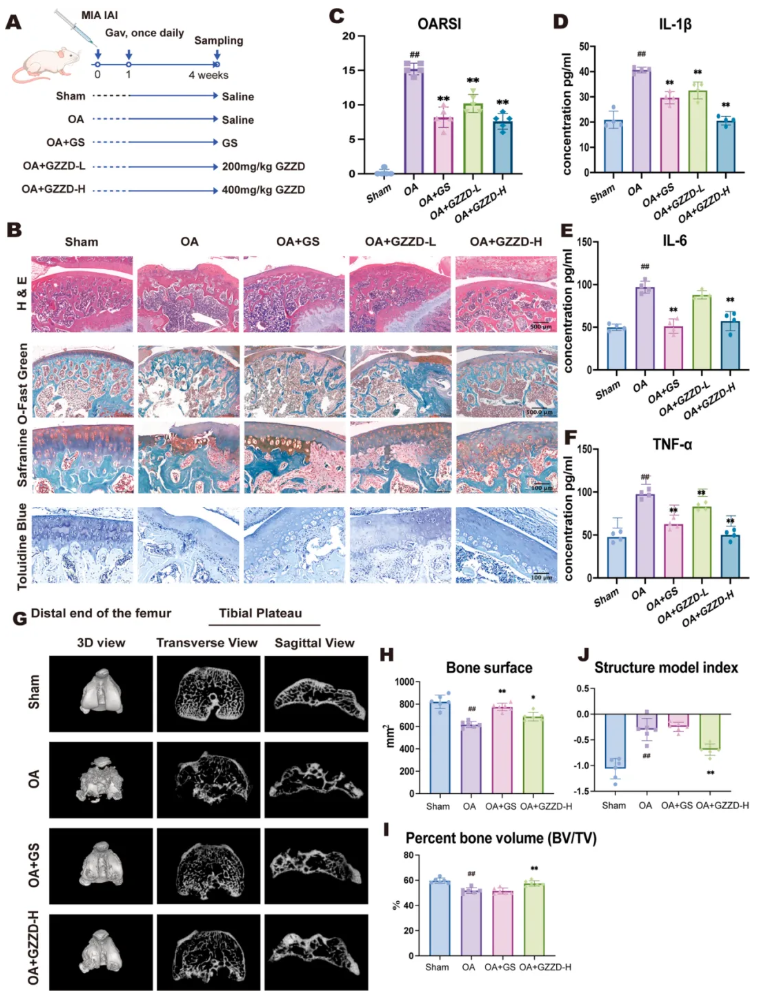
图1. 口服GZZD减轻MIA诱导的大鼠骨性关节炎
02.GZZD对骨性关节炎软骨细胞的保护作用
鉴于GZZD能抑制OA大鼠软骨破坏,该研究选择进一步在软骨细胞层面验证其保护机制,聚焦以下关键蛋白:基质降解酶MMP13、结构蛋白COL2A1、促炎因子IL-1β及抗凋亡蛋白BCL2。结果如图2A-B 所示:OA模型中MMP13与IL-1β显著上调,COL2A1与BCL2明显下调,提示炎症活跃、软骨降解并伴随软骨细胞凋亡;GZZD干预可逆转上述变化,下调MMP13和IL-1β,上调COL2A1与BCL2水平。表明GZZD在体内兼具促合成、抑分解、抗凋亡及抗炎作用,从而减缓OA进展。
为了评估GZZD含药血清对软骨细胞的影响,使用CCK-8法检测细胞活力。CCK-8结果显示,10%及以下浓度均可显著提升原代软骨细胞活力,2.5%浓度效果最佳。在IL-1β诱导的体外OA模型中(图2C-D),中、高剂量含药血清显著抑制MMP13的mRNA与蛋白表达,同时上调聚集蛋白聚糖(ACAN)的mRNA与蛋白水平;空白血清组与模型组间无差异,证实起效的是GZZD活性成分而非血清本身。综上,GZZD在体外同样能缓解IL-1β诱导的OA损伤,进一步支持其作为OA治疗候选药物的潜力。
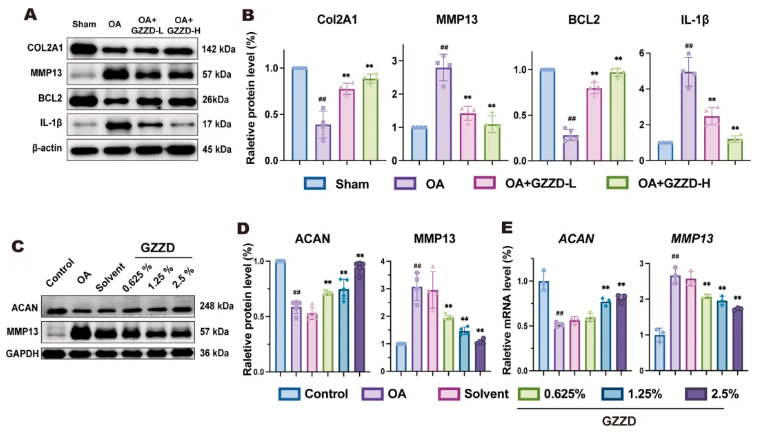
图2. GZZD保护软骨细胞免受OA诱导的损伤
03.GZZD保护线粒体功能,抑制软骨细胞凋亡
在OA中,线粒体自噬受损会导致线粒体功能障碍和凋亡增加,从而加速软骨细胞退变和软骨破坏。透射电镜(TEM)显示,IL-1β诱导的OA软骨细胞出现明显线粒体异常(图3A-B):嵴断裂、内膜肿胀、膜完整性丧失,提示线粒体严重受损。GZZD给药后,线粒体结构、膜完整性及数量均得到恢复。
线粒体损伤可通过线粒体途径触发凋亡,其早期标志为线粒体膜电位(MMP)去极化,表现为JC-1聚合物(红色)/单体(绿色)比值下降。MMP染色显示,与对照组相比,OA软骨细胞红色荧光显著减弱、绿色荧光增强(图3C-D),表明MMP丢失;GZZD以剂量依赖方式恢复MMP,空白血清组与模型组无显著差异。
正常情况下,线粒体通透性转换孔(Mitochondrial permeability transition pore, MPTP)处于关闭状态;线粒体损伤可致MPTP异常开放,钙黄绿素绿色荧光减弱或消失。与对照组相比,模型组绿色荧光显著降低(图3E-F),提示MPTP过度激活;GZZD含药血清剂量依赖性地恢复绿色荧光,表明MPTP活性趋于正常。
氧化应激是线粒体损伤的常见驱动因素,也是OA的标志之一。软骨细胞ROS水平检测显示,模型组绿色荧光强度显著升高;GZZD含药血清各浓度均可显著降低ROS水平(图3G-H)。
软骨细胞凋亡是OA的关键病理特征,且与预后不良反应密切相关,其中线粒体途径起核心作用。Annexin V-FITC/PI染色表明,正常条件下软骨细胞凋亡极少,IL-1β处理后凋亡率显著升高,而GZZD可剂量依赖性抑制IL-1β诱导的凋亡(图3I)。Caspase家族是凋亡的执行者,其活性在凋亡中显著升高。IL-1β显著升高caspase-3、-8、-9活性,GZZD以剂量依赖方式显著降低其活性,与染色结果一致(图3J)。
OA大鼠膝关节软骨TUNEL荧光染色显示,软骨层凋亡细胞显著增多(图3K);GZZD两剂量均显著减少凋亡,表现出强效抗凋亡作用,而阳性药GS仅呈轻微效果。综上,GZZD在体内外均可显著抑制IL-1β诱导的软骨细胞凋亡。
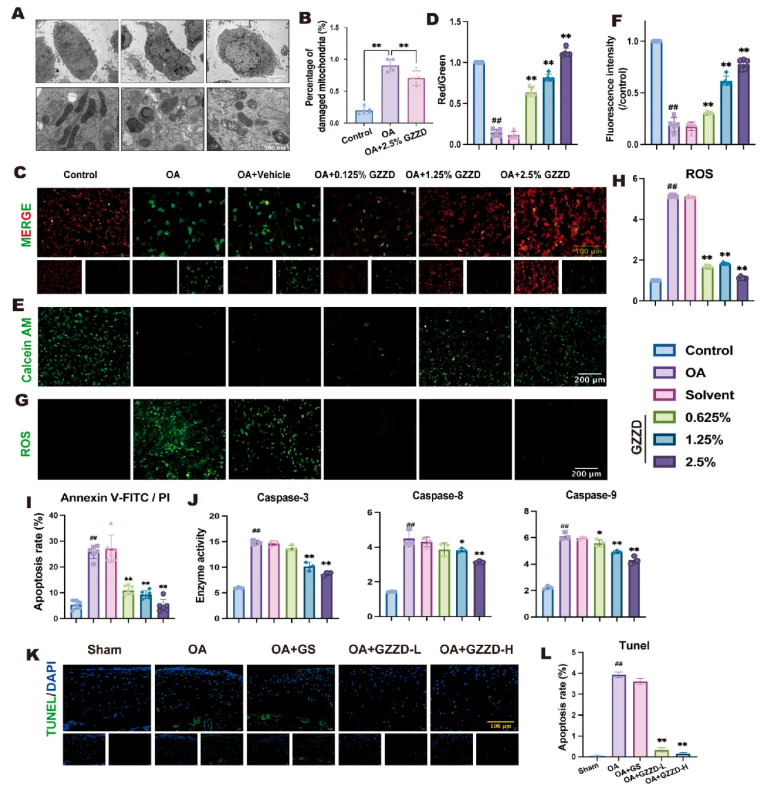
图3. GZZD维持线粒体完整性并抑制软骨细胞凋亡
04.GZZD入血成分鉴定与多组学整合分析
采用高效液相色谱(HPLC)对GZZD提取物进行定性分析,与文献报道的6个质量标志物标准品进行峰对齐验证。结果如图4A所示,GZZD与所有质量标志物完全对应。
随后利用LC-MS/MS鉴定入血原型成分。负离子模式检出49,772个特征峰,鉴定出179种化合物;正离子模式检出45,633个特征峰,鉴定出383种化合物。最终确定61种仅在“GZZD提取物+含药血清”中检出、而对照血清未检出的原型入血成分;经文献及数据库比对,最终确认11种化合物,包括7种黄酮、1种酯类、1种苯丙素、1种萜类及1种酚类。总离子流图(TIC)见图4B-C。
RNA差异表达分析显示:OA vs Sham共得4,500个DEGs;GZZD vs OA获得531个DEGs,其中414个上调、117个下调(图4D)。取Sham-OA与GZZD-OA交集,得到454个共同DEGs。疾病数据库收录5,562个OA相关靶点;GZZD成分预测到240个潜在靶点。将转录组DEGs转换为人源基因后,三者Venny交集获得14个核心靶标(图4E)。KEGG富集提示HIF-1、FoxO和IL-17信号通路与OA密切相关(图4F)。经文献剔除非OA相关通路,结合网络药理学最终锁定11个核心靶蛋白及7个关键活性成分,构建 "成分-靶点-通路" 网络(图4G)。
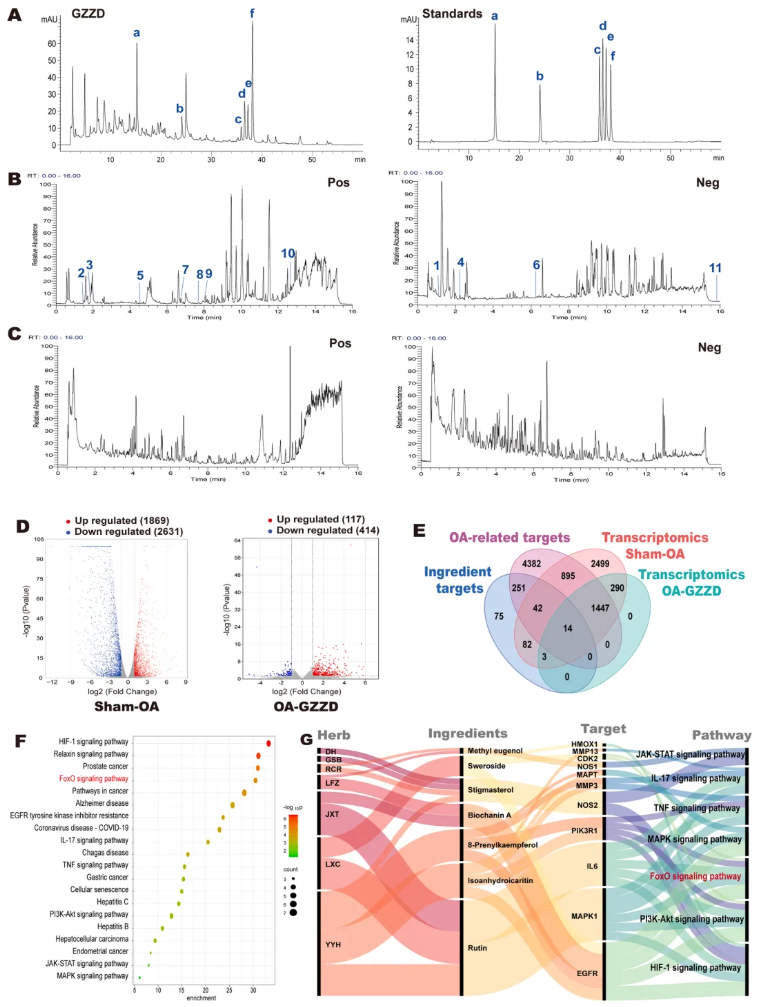
图4. 入血成分鉴定及多组学整合分析
05.GZZD调节FoxO1促进线粒体自噬
线粒体自噬是选择性自噬的一种,可清除受损线粒体、降低氧化应激和炎症,从而保护软骨免受损伤。FoxO1是维持线粒体稳态和自噬功能的关键转录因子,可通过下游调控ATG7、ULK1、PINK1、Parkin等分子介导线粒体自噬,维持细胞完整性。结果显示,IL-1β诱导的OA软骨细胞中FoxO1的mRNA和蛋白表达均显著降低(图5A-C);GZZD处理可恢复FoxO1水平,并在mRNA层面上调其下游靶点ULK1、ATG7、LC3B和PINK1。蛋白检测进一步表明,模型组LC3B、PINK1、Parkin显著下降,P62升高,提示自噬流受阻、线粒体自噬受损(图5D-F);GZZD逆转上述变化,升高LC3B、PINK1、Parkin,降低P62,有效恢复自噬流并激活线粒体自噬,减轻IL-1β诱导的线粒体损伤。此外,在OA大鼠软骨中,GZZD同样显著提升FoxO1、LC3B、PINK1和Parkin的表达(图5G-J)。这些结果共同表明,GZZD通过FoxO1/PINK1/Parkin通路增强线粒体自噬,改善线粒体功能障碍,从而保护OA软骨。
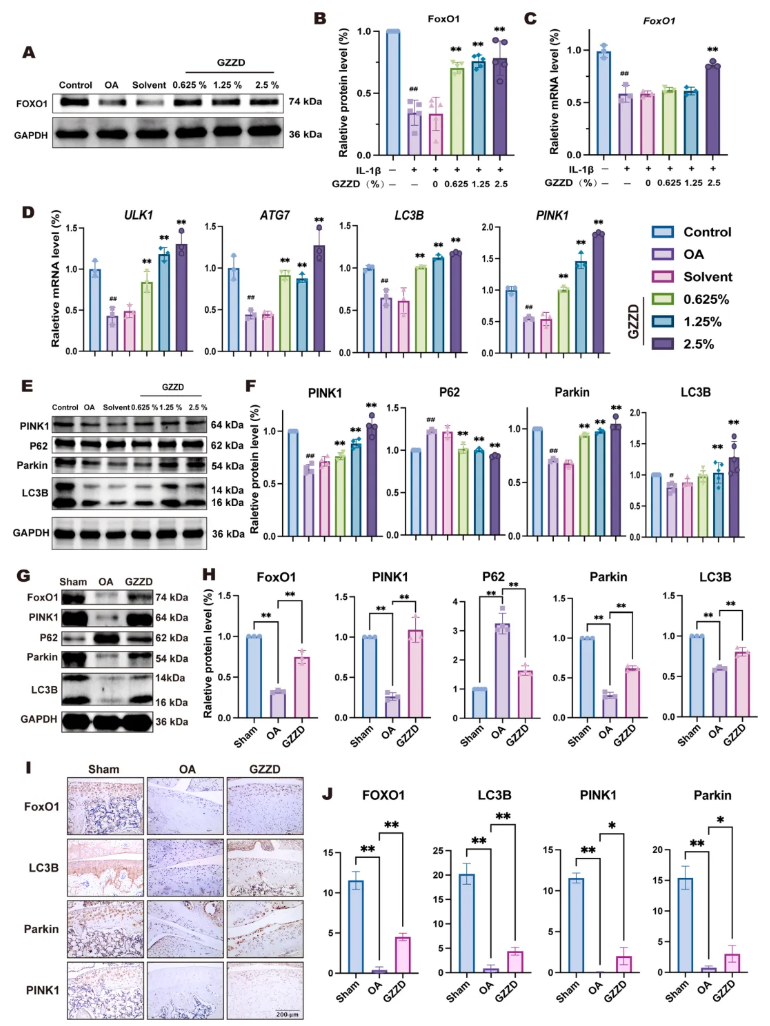
图5. GZZD调控FoxO1激活PINK1/Parkin通路并促进线粒体自噬
06.FoxO1在GZZD介导的软骨细胞保护中的关键作用
为明确GZZD是否通过FoxO1发挥软骨细胞保护作用,采用siRNA沉默FoxO1并观察其对药效的影响。在测试的3个FoxO1-siRNA中,siRNA-3沉默效率最高(图6A-C),被选择用于后续实验。沉默FoxO1后,GZZD对IL-1β诱导OA软骨细胞的保护作用几乎消失(图6D-E):MMP13水平与OA+空载体组相比无显著差异,ACAN表达较GZZD+载体组显著降低,提示保护功能丧失。
进一步检测自噬相关基因发现,FoxO1缺失阻断了GZZD对LC3B、PINK1、ATG7和ULK1转录的调控作用(图6H)。蛋白层面亦证实,FoxO1沉默削弱GZZD诱导的线粒体自噬:LC3-II/LC3-I比值下降、P62升高,PINK1/Parkin通路被抑制(图6F)。上述结果凸显FoxO1在GZZD激活PINK1/Parkin依赖性线粒体自噬中的核心地位。
在线粒体功能方面,FoxO1敲减同样抵消了GZZD的保护效应(图6I-N)。siRNA沉默后,GZZD无法恢复线粒体膜电位、降低膜通透性或减少ROS水平。凋亡实验进一步显示,FoxO1缺失削弱了GZZD的抗凋亡活性:凋亡率升高(图6O)、caspase活性增强(图6P)、BCL-2表达下降(图6G)。综上表明,GZZD抑制OA软骨细胞凋亡主要依赖FoxO1介导的线粒体途径。
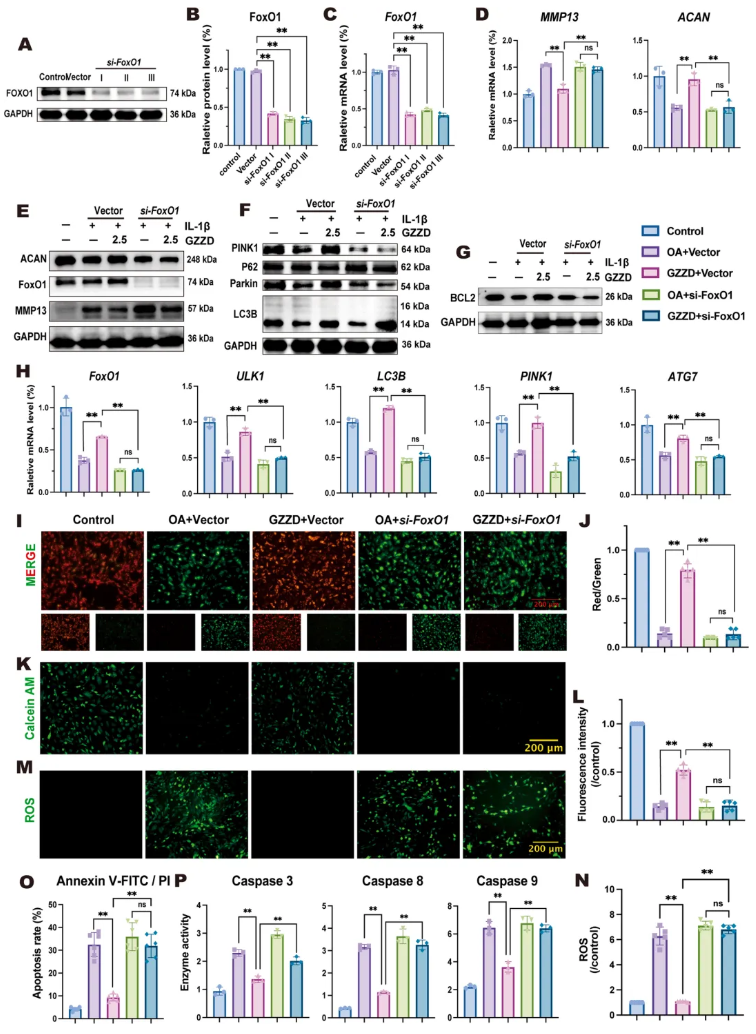
图6. FoxO1在GZZD调控线粒体自噬激活以保护软骨细胞中的作用
研究总结
本研究证实,GZZD可有效缓解大鼠OA进展,在体内外均表现出软骨保护作用,其机制主要依赖于维持线粒体稳态,进而抑制软骨细胞凋亡。GZZD通过激活FoxO1,调控PINK1/Parkin信号通路,恢复线粒体自噬,保护线粒体完整性,从而抑制细胞凋亡,展现出综合治疗潜力。计算机模拟分析进一步预测,芦丁和獐牙菜苷是GZZD中靶向FoxO1的关键活性成分。这些发现不仅为中医疗法治疗OA提供了科学依据,也为开发以FoxO1为靶点的OA治疗策略开辟了新思路。