
文章标题:Extended coverage of human serum glycosphingolipidome by 4D-RP-LC TIMS-PASEF unravels association with Parkinson’s disease
发表期刊:nature communications
影响因子:15.7
研究背景
糖鞘脂(Glycosphingolipids, GSLs)作为细胞膜关键组分,参与细胞识别、信号传导等核心生理过程,其结构与表达异常和免疫疾病、感染性疾病、溶酶体贮积病、癌症及帕金森病(Parkinson’s Disease, PD)等神经退行性疾病密切相关,是疾病机制研究与生物标志物发掘的重要靶点。
然而,传统分析技术受限于GSLs的高度结构多样性、低丰度、异构体分离难度及定量策略缺失,存在通量不足、覆盖度浅、数据库支撑不足等问题,难以实现临床样本中糖鞘脂组的系统解析,无法全面揭示其与疾病的关联。在此背景下,开发高灵敏度、高覆盖度、高通量且能精准区分异构体的糖鞘脂组学分析平台成为关键需求。
本研究引入4D-RP-LC TIMS-PASEF MS技术,通过整合反相液相色谱(RP-LC)、捕获离子淌度谱(TIMS)与平行累积连续碎裂质谱(PASEF),以质荷比(m/z)、保留时间(RT)、碰撞截面(CCS)、MS/MS质谱为四维特征,实现中性GSLs、唾液酸化GSLs及硫脂的全面覆盖,突破传统技术瓶颈,为深入解析糖鞘脂组与PD的关联提供全新技术支撑。
研究结果
01.4D-RP-LC TIMS-PASEF糖鞘脂组学平台的分离策略与方法优化
首先,针对传统聚糖基分离技术(如HILIC/正相色谱)中存在的同位素体重叠问题(相似聚糖结构但不同神经酰胺链的GSLs共洗脱),本研究尝试以RP-LC基于神经酰胺疏水性分离GSLs。经方法优化后发现,“关闭在线校准、开启TIMS” 能有效提升电离效率与检测灵敏度。结果显示,不同GSLs生成特征离子(如GM3/GM2为[M−H]⁻,GD/GT/GQ为[M−2H]⁻,GP为[M−H₂O−2H]²⁻),RP-LC依据神经酰胺结构(链长、饱和度、羟基化)及糖基化/唾液酸化修饰程度实现有效分离(图1b);TIMS可在正负离子模式下对GD1a/GD1b异构体完成部分分离(图1c),与RP-LC的色谱分离形成正交互补;二者结合的RP-LC-TIMS-PASEF碎裂技术(正离子模式解析神经酰胺组成,负离子模式解析聚糖结构)能精准匹配神经酰胺组成与聚糖结构。
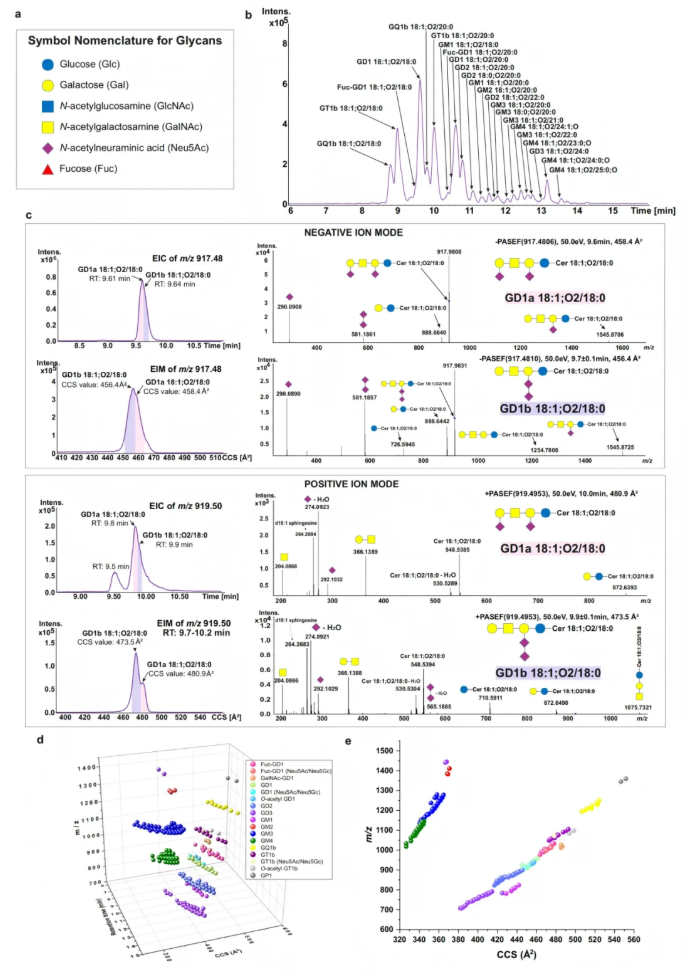
图1. 利用RP-LC TIMS-PASEF开展的四维糖鞘脂组学分析
此外,各糖鞘脂亚类在m/z-RT-CCS三维空间(图1d)和m/z-CCS二维维度(图1e)中形成专属区域,实现近乎基线的区分,这既解决了同位素体重叠的定量难题,也为未知GSLs的从头鉴定奠定基础。更惊喜的是,在定制的标准品中还鉴定出Fuc-GD1、GalNAc-GD1等新亚型(图1c, 图2a-c),并在猪脑提取物中鉴定出47种分属17个亚类的神经节苷脂(图2d),为该样本中已报道的最高鉴定数量。以上结果证实,4D-RP-LC-TIMS-PASEF对中长链、高唾液酸化,以及岩藻糖基化、O-乙酰化修饰的糖鞘脂,具备优异的高灵敏度检测和高分辨率分析能力,为后续复杂生物样本的糖鞘脂组学分析筑牢技术基础。
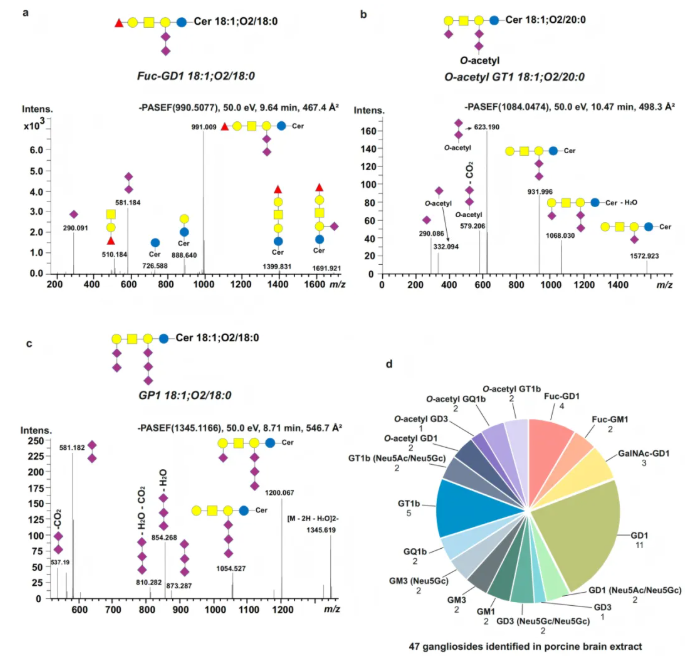
图2. 标准品与猪脑提取物中O-乙酰化/岩藻糖基化/五唾液酸化糖鞘脂的代表性PASEF谱图
02.4D糖鞘脂数据库的构建及自动化注释应用
当前,GSLs结构表征存在着数据库缺陷的核心难题:注释数据库缺乏实验碎裂光谱,复杂修饰型GSLs(如岩藻糖基化、O-乙酰化修饰GSLs及五唾液酸神经节苷脂GP等)无虚拟碎裂数据支撑,且现有数据库仅含简单GSLs亚型,数据为虚拟模拟生成,缺失生物基质和溶剂效应信息,无法实现生物样本中高可信度的GSLs注释与中高通量分析。
为解决这一问题,研究基于商用标准品和猪脑提取物,构建了首个基于4D-RP-LC TIMS-PASEF技术的、包含保留时间(RT)、碰撞截面积(CCS)、质荷比(m/z)及PASEF质谱的四维(4D)实验数据库。该数据库共收录226种神经节苷脂,命名为“4D-sialoGSL standards library”,通过关联多维度参数形成分析物列表,为血清GSLs注释提供核心依据。
03.人血清中糖鞘脂的微量提取
研究前期开发的血清GSLs提取方法虽然能从300 µL血清中提取中长链唾液酸化GSLs,但需依赖nanoflow HPLC/nanoESI-QTOF MS的灵敏分析,且长链物种主要在合并提取物中才能检出。为匹配4D-TIMS-PASEF平台的高通量和高灵敏度,本研究对此方法进行了系统性优化。
优化后的提取流程包括:磷酸甘油酯去除、反相纯化,以及关键的硅胶分级步骤(图3a)。其中,原方法的 “四步” 硅胶分级被简化为 “两步”,分别富集组分1(中性GSLs、硫脂、GM3)和组分2(复杂唾液酸化GSLs)。相比 “四流程法”(135种),“两流程法” 能够检测到更多复杂的GSLs(147种,图3b),同时也显著缩短了样品处理、分析与数据处理时间,降低了半定量的变异性,并减少了样品损失。
此外,简化分级的另一重要考量是内标的跨组分分散问题。由于GSLs(尤其GT、GQ等类别)的氘代内标极为匮乏,必须使用跨类内标。然而,原多步分级易导致内标分散于不同组分,干扰半定量。对此,本研究评估了四种内标(GD3-d3、GM1-d5、GM2-d9、GM3-d5)在两组分间的分配比例(图3c)。结果显示,其在组分2中的分配比例稳定且重现性良好(四种内标占比70.35%-80.40%,CV均低于7.5%),验证了优化方法的有效性,为后续血清GSLs半定量奠定了基础。
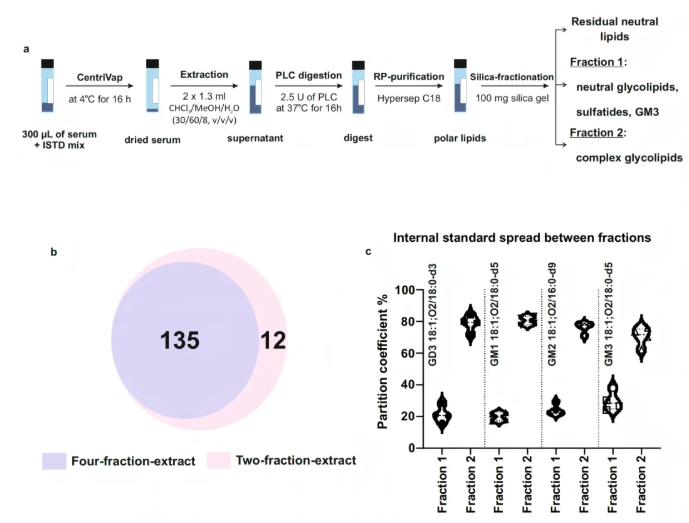
图3. 微量提取人血清中的GSLs
04.人血清糖鞘脂组
为验证GSLs微提取与4D糖鞘脂组学联用体系的分析性能,本研究对NIST 1951c标准血清及志愿者血清进行了分析。结果显示,所建立的血清GSLs提取方法(图3a)结合µL-flow RP-LC-TIMS-PASEF技术,在唾液酸化GSLs结构异质性覆盖方面显著优于传统nanoflow LC-MS(图3d)。这一提升主要得益于两步分馏策略(图3b)及RP-LC与TIMS联用带来的结构分辨能力增强。TIMS能有效分离RP-LC无法区分的同分异构体(如GM1与Neu5Ac-nLc4Cer),结合PASEF碎裂谱实现明确结构解析(图4a),充分体现离子迁移与液相色谱的正交分离优势。
在血清组分2中,共鉴定出159种唾液酸化GSLs,覆盖20个亚类,创人血清中唾液酸化神经节与新乳糖系列鉴定数量新高。负离子模式下PASEF保留高唾液酸化结构并清晰解析糖链构型(图4b-c);正离子模式则可明确神经酰胺脂肪酰链与鞘氨醇碱基类型。在组分1中,145种中性GSLs与72种硫苷脂被鉴定(图5),PASEF同样可准确推导其糖链与神经酰胺结构(图4d-e)。
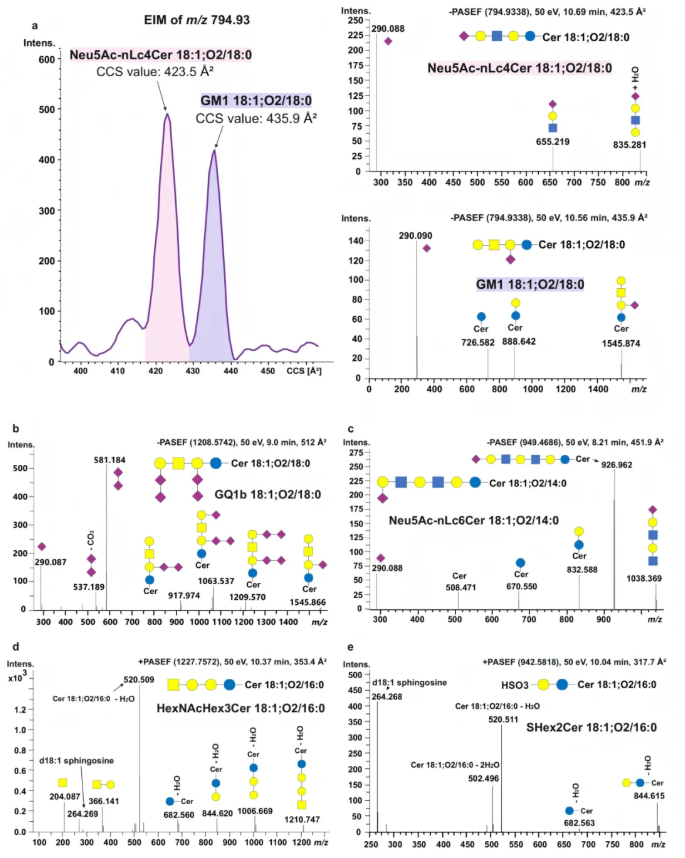
图4. 人血清中GSLs的代表性PASEF质谱图
此外,该平台还成功检出Fuc-GD1、O-acetyl GD1、GQ1b等低丰度及高修饰GSLs,实现nLc4-nLc12长链新乳糖系列与人血清硫苷脂的广泛覆盖。RP-LC与IMS的互补分离在三类GSLs中表现明显:IMS区分糖链构型,RP-LC分辨神经酰胺组成(图5)。同时,该平台通量较高,24样本可在2.5天内完成全流程分析。基于鉴定结果,研究还构建了首个4D-TIMS-PASEF糖鞘脂组综合实验质谱库,以及血清唾液酸化、中性GSLs及硫苷脂三个4D数据库,为各类样本中GSLs的自动化、高可信度注释提供重要支撑。
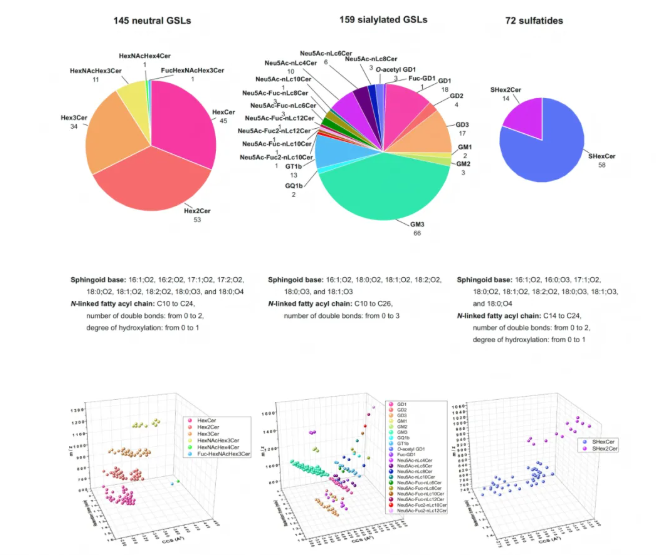
图5. 基于µL-flow 4D-RP-LC-TIMS-PASEF技术鉴定的人血清GSLs组
05.人血清中唾液酸化GSLs的半定量策略
为实现单个血清样本中唾液酸化GSLs的可重现半定量,本研究针对内标匮乏、跨组分分配及数据处理难题,设计了两种定量策略(图6a)。其中,策略I基于对照血清中内标的平均分配系数(6次提取)计算样本含量;策略II则使用每个样本内标的实际分配系数,但需分析两个组分,增加耗时。除此之外,两种策略结合三种内标组合的 “子策略”(图6b)也一并被评估,采用35%变异系数(CV)为阈值。
结果显示,策略I初始CV<35%的物种比例较低,主要因两个离群样本的内标分配异常。排除1个离群值后,比例提升至67.21%-76.23%;排除2个离群值后进一步提升至84.42%-87.80%。策略II在未排除离群值时,CV<35%物种比例已达66.39%-70.49%,整体优于基于平均分配的策略I,但需分析两组分。三种内标组合中,“子策略三” 结果最稳定、离群值最少,表明待测物与内标行为一致。
综合考量,推荐采用 “子策略三结合策略II”,离群样本可用策略I校正。校正后,72.95%的物种CV<35%,多数亚类平均CV低于 30%(图6c)。方法学验证显示,主要GSL亚类线性R²>0.97,检测限(LLOD)达低fmol级,定量限(LLOQ)为高fmol 级。GD1的LLOQ最高,可能因其GD1a/GD1b异构体共存(图6d)。平均残留效应仅1.2%。组分1中性GSLs和硫苷脂的半定量采用内标GM3 18:1;O2/18:0-d5的峰面积归一化。
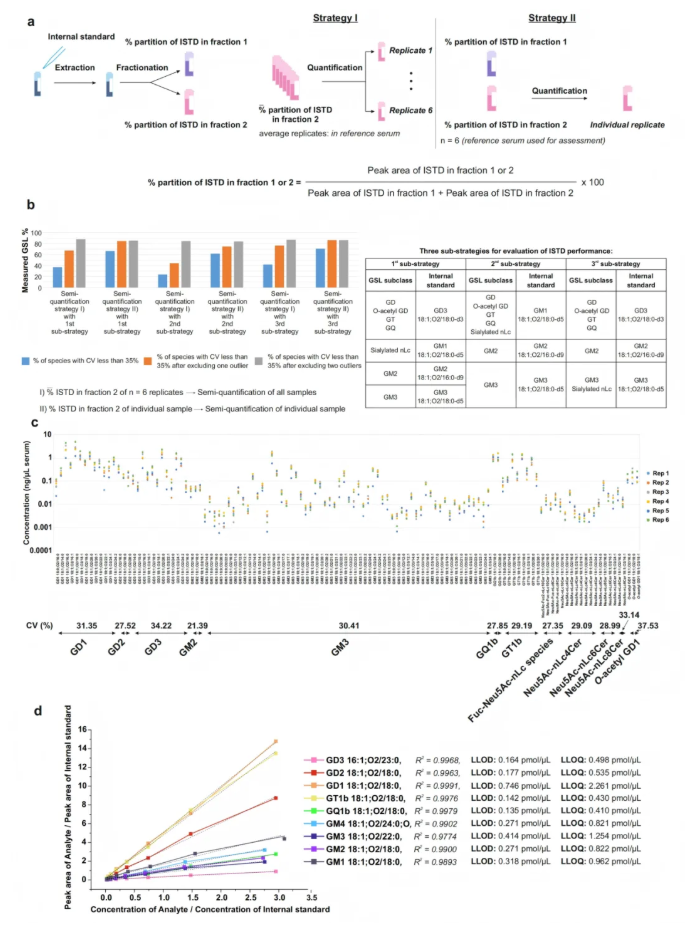
图6. 人血清中唾液酸化GSLs的定量策略
06.帕金森病中GSLs的表达变化
帕金森病以α 突触核蛋白聚集为典型特征,GBA1突变及GCase活性降低是重要危险因素,但既往研究缺乏GSLs分子层面的系统解析。研究对30例健康对照与28例PD患者血清进行GSLs分析,共鉴定出98种唾液酸化GSLs、145种中性GSLs及72种硫苷脂,分子覆盖C10-C24脂肪酰链及多种神经酰胺结构类型。以性别和年龄为协变量的统计分析显示,PD组共有41种GSLs显著上调,主要包括39种神经节系列(GM3、GM2、GD3、GD1等)以及2种唾液酸化新乳糖系列(nLc4、nLc6),表明相关糖基转移酶通路出现异常活化(图7a-b)。
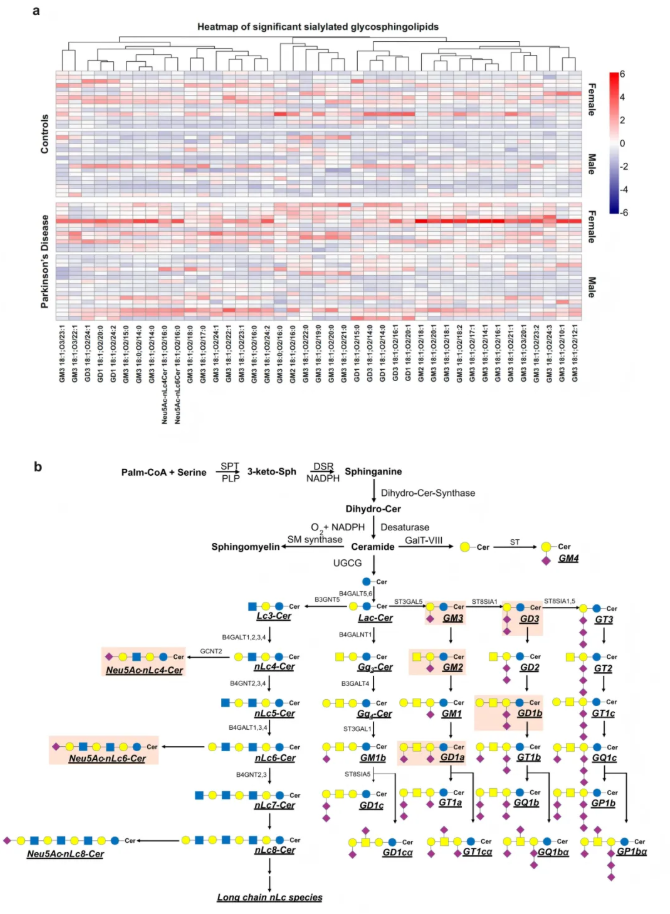
图7. 帕金森病中唾液酸化糖鞘脂的表达特征
进一步分析发现,PD患者GSLs表达存在显著性别差异,多种GM3亚型、GD1系列及新乳糖系列分子在男女患者间呈相反变化趋势(如女性GT1b、部分GM3 亚型升高,男性GD1系列升高,O-acetyl GD1呈反向改变),与临床中男女PD易感性及病程进展差异相吻合,证实本方法可稳定反映临床表型(图8a-b)。HexCer水平无明显改变,与受试患者未携带GBA1突变相一致;下游延伸中性GSLs(Hex2Cer、Hex3Cer、HexNAcHex3Cer)显著上调,变化趋势与唾液酸化GSLs一致。硫苷脂亚类整体无显著差异,仅部分SHexCer分子水平存在改变(图8c-d)。
综上所述,本研究系统揭示了PD相关的GSLs异常谱,为PD生物标志物筛选及病理机制研究提供重要依据。
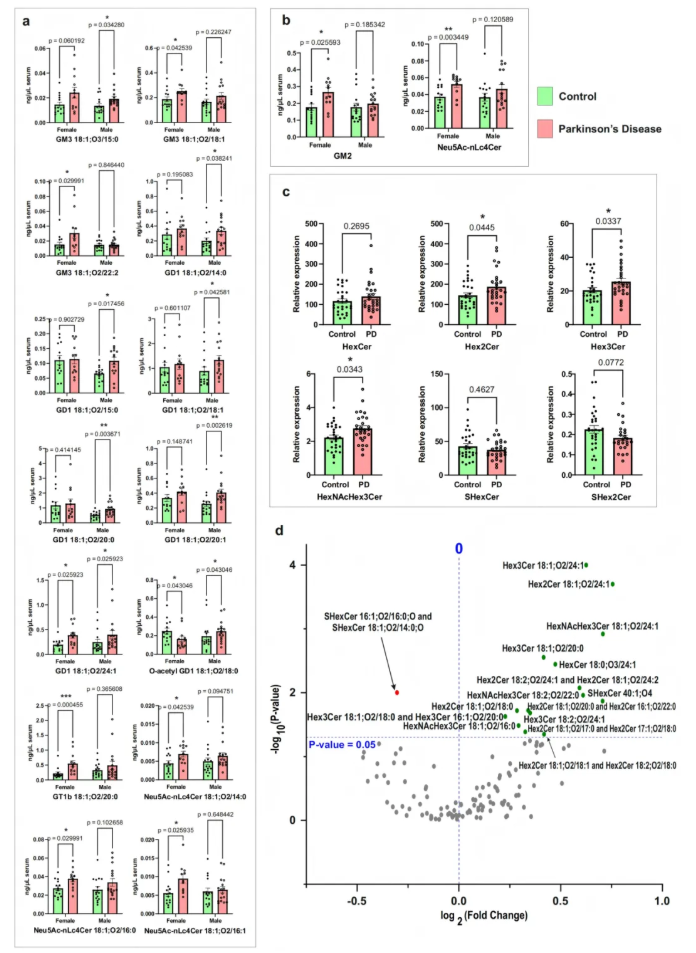
图8. 健康对照组与帕金森病组的糖鞘脂差异定量特征
研究总结
本研究搭建的4D-RP-LC-TIMS-PASEF技术平台,搭配专属4D数据库实现了糖鞘脂(GSLs)的自动化高可信度注释,为临床脂质组学研究提供了强力支撑。依托该平台,成功在人血清中鉴定出376种GSLs(159种唾液酸化GSLs、145种中性GSLs及72种硫脂),大幅拓展了复杂脂质的覆盖范围。在帕金森病(PD)临床应用中,该平台展现出卓越价值:锁定41种在PD患者中显著上调的GSLs,同时发现14种存在性别差异的GSLs,清晰揭示了PD相关的GSLs异常谱及潜在代谢通路。这一成果不仅为PD生物标志物筛选与病理机制研究开辟新路径,更充分印证了4D脂质组学技术在神经退行性疾病及多类疾病研究中的广阔应用前景,为临床转化研究提供了有力支撑。