
文章标题:Multi-omics microsampling for the profiling of lifestyle-associated changes in health
发表期刊:nature biomedical engineering
影响因子:26.6
研究背景
多组学技术已成为解析健康与疾病分子机制、挖掘血液生物标志物的核心手段,但其在纵向追踪、动态机制研究中的应用,仍受传统样本采集技术制约:传统静脉采血需专业操作、样本需求量大,无法实现高频采样,难以捕捉生物体系中 “分钟-小时级” 的分子动态变化。
现有主流微采样技术(如干血斑DBS)虽尝试突破采样场景限制,却存在体积重复性差、检测靶标有限等问题,无法高效兼容代谢组、脂质组、蛋白质组等多组学同步分析,难以满足科研对多维度分子数据的挖掘需求。
在此背景下,10 μl指尖血多组学微采样技术应运而生,仅需微量血样即可实现代谢物、脂质、蛋白质等多类分子的高通量检测,既保留多组学全面解析分子网络的优势,又以微量、高频特性突破传统采样的时空与体积限制,为多组学技术在生命科学研究中的规模化、深度化应用提供了关键技术支撑。
研究结果
01.多组学微量采样方法的概述
本研究建立了一套多组学微量采样分析体系,核心流程如图1a所示:采用Mitra固体基质装置采集10 μl固定体积的指尖血样本,经多种提取条件筛选后,确定采用甲基叔丁基醚(MTBE)双相提取法,从单份微量样本中同步分离:有机相(含疏水代谢物与脂质)、水相(含亲水代谢物)及甲醇沉淀的蛋白质沉淀(用于蛋白质组学分析);同时另取一份微量样本经水相提取,在Luminex平台完成多重免疫检测(细胞因子/激素),随后对蛋白质组、代谢组、脂质组及细胞因子组学数据进行标准化处理、注释与质控(QC),用于后续深度分析。
方法学验证方面,分为三步展开(图1b):①测试不同储存温度与时长下蛋白质、代谢物、脂质三类分子的稳定性,证实多数分析物可稳定检测;②与传统静脉采血对比,验证分子检测结果的一致性;③通过两项试点案例研究,验证技术在真实生活场景中捕捉健康与生物学扰动的实用性。
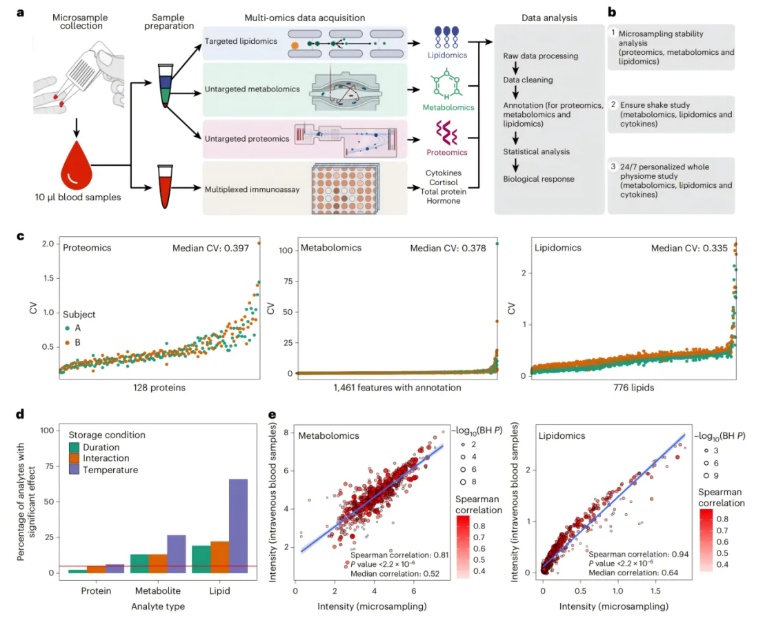
图1. 微量采样多组学工作流程与稳定性分析概述
02.代谢物、脂质和蛋白质在多种条件下的微量样本稳定性
首先,针对微量样本中蛋白质、代谢物和脂质在多种条件下的稳定性,研究采集了两名健康者的指尖血微量样本(每份10 μl),分别置于4℃、25℃和 37℃条件下储存,设置3、6、24、72、120小时五个时间梯度,同时设置一组样本采集后立即置于-80℃储存作为基线,所有样本最终均在-80℃冻存至分析。随后对所有样本进行多组学检测,并通过三种指标评估其分子稳定性:①两组受试者样本的平均变异系数(CV);②线性回归分析储存条件(时间、温度及二者交互作用)对分析物水平的显著影响;③相对重要性度量(图1c-d)。结果表明,绝大多数分析物在不同储存条件下保持稳定。
03.微量样本与静脉血浆样本的比较
研究纳入34名受试者,系统对比了微量全血采样与传统静脉血浆采样在多组学检测中的一致性(图1e)。所有受试者均在空腹状态下同时采集微量全血样本与静脉血浆样本,立即置于-80℃冻存,后续采用相同流程进行非靶标代谢组学(涵盖亲水/疏水代谢物)与靶标脂质组学检测。
结果显示,两种采样方法的分子检测结果高度一致:非靶标代谢组学检测的642种代谢物Spearman相关系数达0.81,靶标脂质组学检测的616种脂质Spearman相关系数达0.94。大多数分子类别(包括大部分氨基酸、碳水化合物、游离脂肪酸、甘油三酯、二酰甘油、磷脂酰胆碱等)的检测结果高度相似,无显著系统性差异,证实微量采样可支撑可靠的非靶标代谢组学检测。
04.多组学微采样技术的案例应用验证
为进一步验证多组学微采样技术在真实科研场景中的实用性与优势,研究设计了两项试点案例研究:一是聚焦饮食干预的个体化代谢响应分析,二是结合可穿戴设备的高频动态生理-分子关联解析,具体如下:
4.1 饮用Ensure奶昔后的代谢表型反应
鉴于传统采血方法难以实现高频采样、无法捕捉进食后快速变化的代谢动态等痛点,研究利用微量采样法,开展了针对Ensure奶昔摄入的代谢响应案例研究。
28名背景多样的受试者参与了高时间分辨率的监测(图2a)。通过代谢组、脂质组、细胞因子与激素检测,最终获得560种代谢物、155种脂质、54种细胞因子/激素,共768个分析物,合计140个数据点(图2b)。具体实验内容及结果主要如下:
(1)差异分子的聚类分析
为探究机体对Ensure奶昔的分子响应特征,研究首先通过Wilcoxon检验分析了各时间点与基线相比发生显著变化的分子(图2c)。结果显示,大多数显著上调的代谢物与脂质在摄入后,分别于60min、120min达到峰值,并均在240 min基本恢复基线水平。
透过方差分析量化受影响的分子数量,结果发现,奶昔摄入后,17.7%的代谢物、74.2%的脂质和13.0%的细胞因子/激素水平发生显著改变。其中,变化分子的信号强度显著高于储存条件带来的影响,证实了数据的生物学有效性。
基于模糊c均值聚类,这些显著变化的分子可被划分为3个时序簇(图2d):“簇 1”快速上升并在60min达峰,“簇 2”平缓上升并在60-120 min达峰,“簇 3”摄入后先下降后回升。
(2)Ensure奶昔引发的代谢通路改变及生理反应
根据上述分子聚类结果,Ensure奶昔引发的代谢通路与生理响应被进一步解析(图2d)。
在代谢方面,“簇 1”以氨基酸、碳水化合物为主,富集氨基酸代谢相关通路,多直接来自奶昔并快速响应(图2e-f);“簇 2”主要由甘油三酯构成,其响应较慢,展示了脂质代谢的独特动力学;“簇 3”以乙酰肉碱和游离脂肪酸为主,摄入后下降,反映了能量稳态调节(图2g)。
对于激素和细胞因子,其变化也呈现出明显的聚类特征(图2h)。其中,胰岛素、C肽、GIP等同步升高,瘦素、IFNG、IL4下降,表明奶昔具有潜在的抗炎效应。
此外,结合质谱分析,Ensure奶昔中近50%的成分可在血液中被检出,21种关键变化代谢物里就有17种来自奶昔,证明微量采样可有效捕获摄入的分子特征,依托10 μl微量血样的非靶标代谢组学检测,能精准还原饮食干预后的体内代谢动态变化。
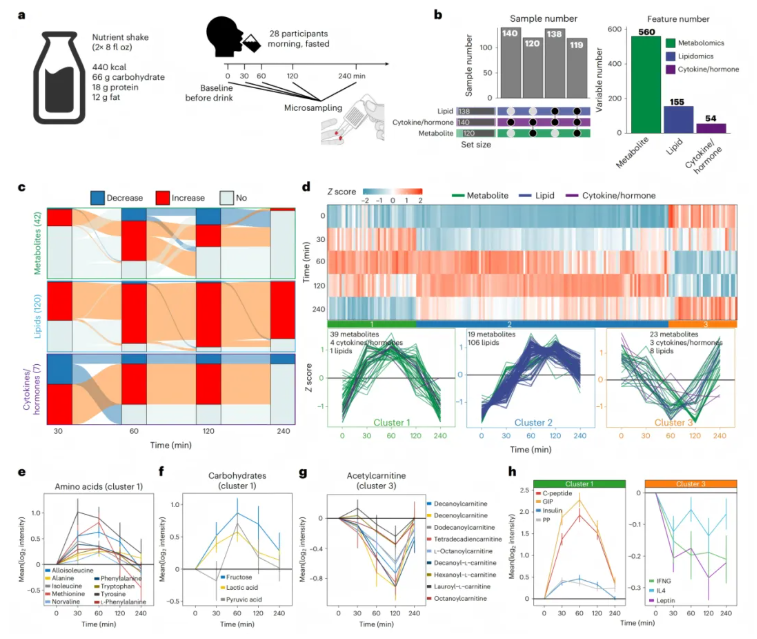
图2. Ensure奶昔研究概述以及相关的分子反应
(3)代谢表型分析揭示独特的个体应答
个体对不同食物的应答差异是研究热点。Ensure奶昔虽为成分明确的标准化营养制剂,却包含多种可被小肠快速吸收的小分子复合物。研究透过t-SNE降维分析、无监督共识聚类法、胰岛素抵抗指标(SSPG)等方法(见原文扩展数据图2),证实了个体对Ensure奶昔的分子应答具有高度独特性:t-SNE分析显示样本按受试者聚类,个体间差异大于饮食干预效应;无监督共识聚类将受试者分为2组,组2的代谢应答速率显著慢于组1,且胰岛素抵抗受试者更倾向归为组1。
这一结果表明,微量多组学采样技术可高效捕捉这些个体化代谢表型——其低创、高频的特性,解决了传统静脉采血无法实现高频动态监测的痛点,能精准还原个体在饮食干预下的独特代谢响应,为精准营养方案制定、代谢疾病风险分层与个性化干预提供重要科学依据,也印证了微量非靶标代谢组学在个体化研究中的核心价值。
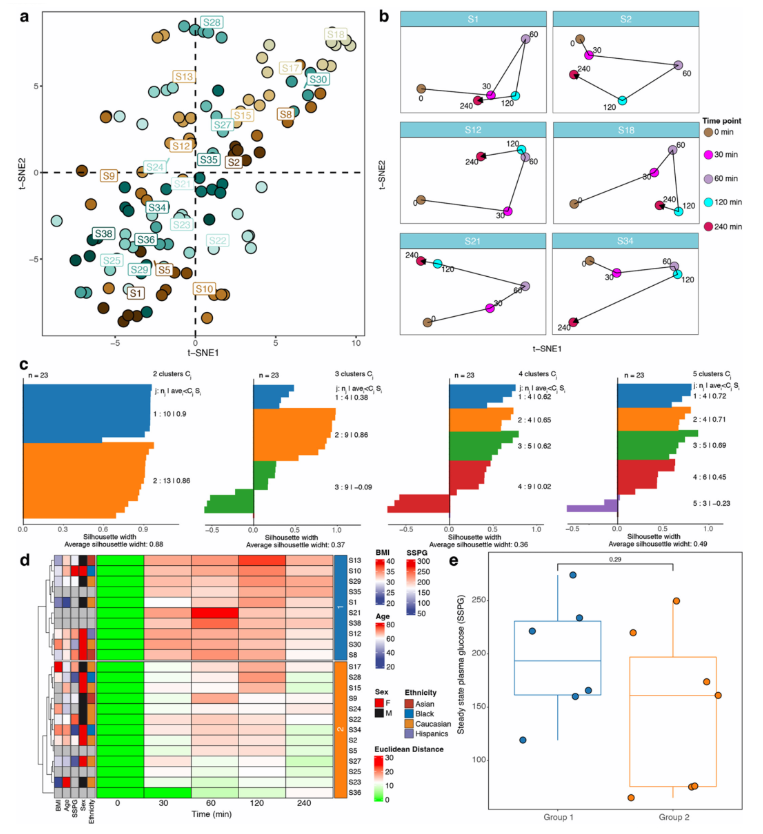
扩展数据图2. 代谢表型分析区分个体差异与饮食干预的代谢响应
(4)基于Ensure奶昔动态应答的代谢评分
基于摄入后各分子的动态变化曲线下面积(图3a),研究构建了六项代谢评分系统,分别对应碳水化合物、脂质、游离脂肪酸、氨基酸、胰岛素分泌及细胞因子炎症反应,明确了每项评分对应的核心分析物(图3b)。
依据六项代谢评分的层次聚类分析,可将受试者划分为5组(图3c),不同组别在各类分子的应答强度上存在明显区别(图3d)。例如,部分个体脂肪与氨基酸代谢应答较弱(如第1组的S30),部分则碳水化合物与氨基酸代谢应答更强(如第5组的S34);还有个体呈现显著的激素或炎症因子高应答(如第5组的S35),提示个体对营养物的应答存在多维度异质性。
总的来说,个体对复合营养物的生化反应涉及代谢、免疫、内分泌等多系统的复杂差异,远非单一指标所能概括。对此,微量采样技术凭借高时间分辨率的优势,能够精准捕获这些复杂的个体代谢特征,为量化个体营养应答差异提供了可靠工具,也为未来实现真正意义上的精准营养干预提供了关键的技术手段和数据基础——这一结果进一步印证,依托该技术的微量非靶标代谢组学,可深度支撑个体化营养研究与精准医疗应用。
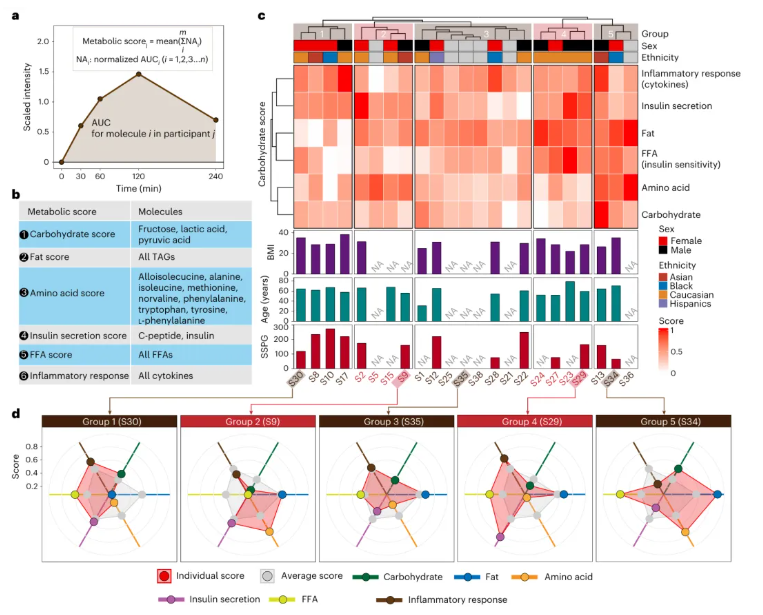
图3. 基于Ensure奶昔多组学应答的代谢表型分析
4.2 利用可穿戴设备与多组学数据进行“24/7”个性化全身生理组分析
为验证 “高频微量采样+可穿戴设备” 在真实生活场景中挖掘生理-分子关联的可行性,研究将微量采样技术与可穿戴设备结合,对1名64岁男性受试者开展了7天的个性化全身生理组分析(简称 “24/7研究”)。
受试者清醒时段每1-2小时采集10 μl微量血样(部分采样间隔缩短至30分钟),7天累计采集98份样本(图4a)。最终,2213种分析物被成功检测,包含1051 代谢物、811种脂质、291种蛋白质、45种细胞因子等(图4b);结合可穿戴生理数据(心率、步数、连续血糖、睡眠状态等),累计获得214661项生化与生理测量数据,构建了小时级的人体全身生理组与生活方式纵向数据集(图4b-c)。后续实验内容及结果主要如下:
(1)可穿戴设备数据与体内多组学数据反映个体生理状态
在“24/7 研究”中,通过模糊c均值聚类分析对2213种内源分子进行分类,识别出11种主要的时间变化模式(图4d)。其中,簇4(富含代谢物)的分子水平普遍在日间达峰,簇11(以脂质为主)的分子水平主要在夜间达峰,二者表现出明显的昼夜节律特征;其余簇的分子变化不依赖昼夜周期,推测对应饮食、运动等非节律性特定生理事件。
通过群落分析从各簇中提取核心分子模块,发现部分模块存在明显的表达峰值(图5a),暗示这些模块中的分子变化由特定生理事件(如饮食摄入、药物服用、炎症反应等)触发。另外,结合每日饮食记录进行关联分析,发现氨基酸、脂肪类营养素与多个富集氨基酸、游离脂肪酸、脂质的分子模块高度相关,且精准捕捉到 “晨起饮用代餐奶昔” 与血液中1,2,3-苯三酚硫酸盐、羟苯乳酸(奶昔特征化合物)水平升高的直接关联,证实微量采样技术可可靠捕获饮食摄入后的分子应答特征——这一结果进一步印证,依托该技术的微量非靶标代谢组学,能精准还原真实生活场景下的个体代谢动态。
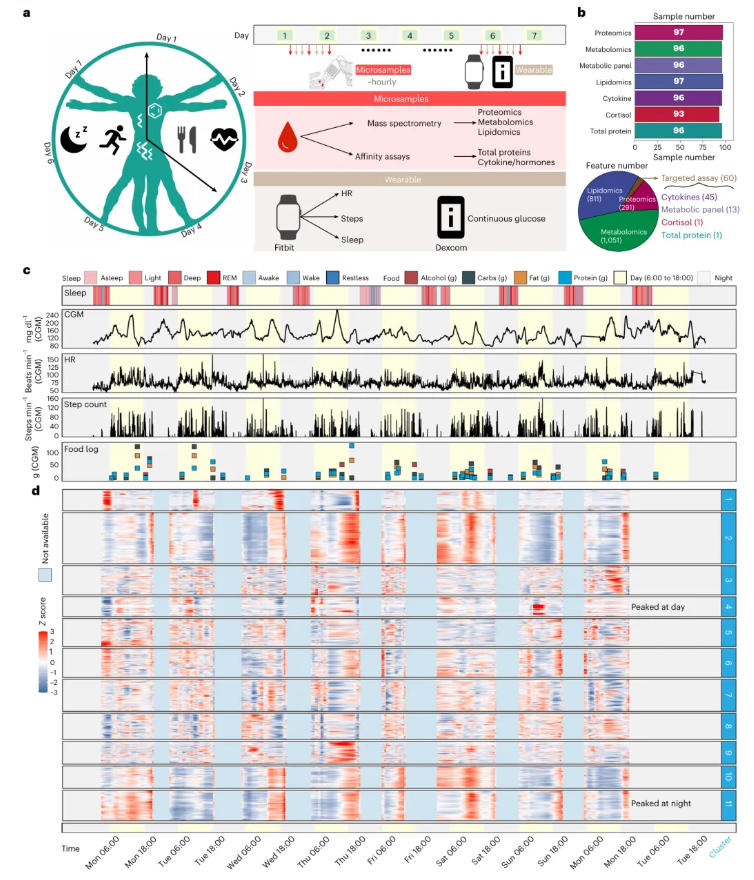
图4. 24/7研究的实验设计、样本采集及数据采集概述
(2)人体血液内部分子的昼夜节律
借助微量采样获得的高时间分辨率高频数据,人体血液中332种具有显著昼夜节律的分子被系统解析(图5)。研究通过筛选具有稳定日周期模式的分子,发现具有完整24小时周期的节律分子主要归为三类(图5b-c):“聚类1” 以磷脂酰胆碱(PC,占比32.56%)和溶血磷脂酰胆碱(LPC,占比25.58%)为主,“聚类2” 几乎完全由甘油三酯(TAGs,占比93.65%)构成,“聚类3” 则同时富含甘油三酯(TAGs,占比49.15%)和磷脂酰乙醇胺(PE,占比22.03%)(图5d)。三类聚类的典型分子示例详见图5e,其节律模式与能量代谢密切相关,且不受饮食脂肪摄入驱动,推测由个体内在节律动力学或肠道微生物调控。
这一结果证实,微量非靶标代谢组学可精准捕获血液中节律分子的动态特征——依托10μl微量血样的高频采样与高通量检测,能系统揭示传统采血无法捕捉的昼夜节律分子谱,为生物钟机制研究、代谢节律相关疾病(如睡眠障碍、代谢综合征)的标志物筛选提供了关键技术支撑。
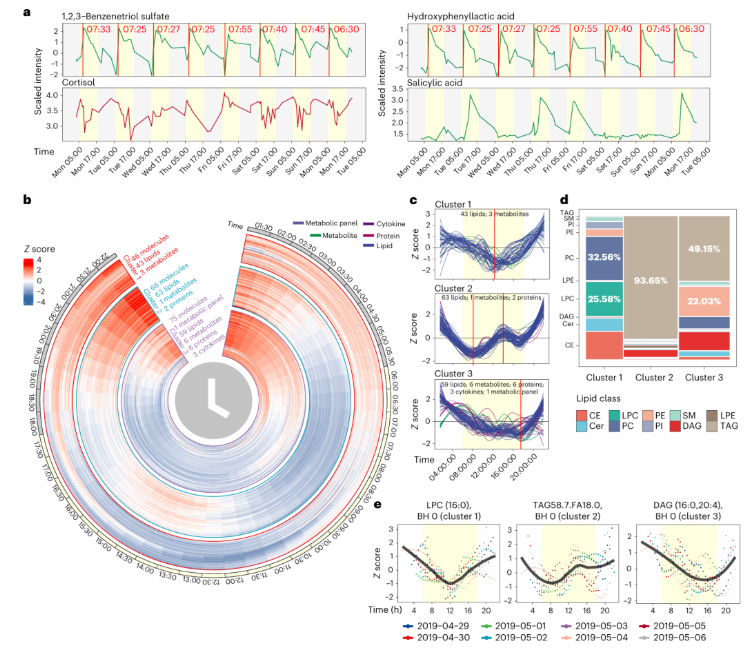
图5. 可穿戴设备与体内多组学数据的个体生理状态表征及多组学数据的昼夜节律分析
(3)可穿戴设备数据反映体内分子变化
聚焦可穿戴设备数据与体内分子变化的关联,研究基于多组学数据与滞后相关分析,结合高频微量采样与laggedCor算法(R包),构建出CGM葡萄糖子网络(图6a)。结果而言,α-突触核蛋白可能直接或间接上调血糖水平;CGM葡萄糖变化早于C肽10分钟,符合生理预期;CGM与多种促炎细胞因子呈显著滞后相关,表明血糖升高可快速触发特异性促炎反应(图6b)。
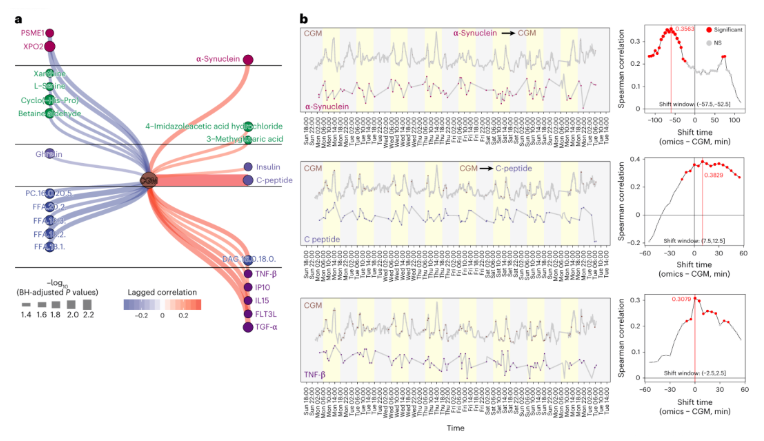
图6. 持续血糖监测(CGM)与体内分子的因果关联网络
研究总结
本文开发了一种基于10 μl血液微量采样的多组学分析策略,通过Mitra装置采集样本并结合MTBE双相萃取法,可同步提取蛋白质、脂质、代谢物等多类分子。经不同储存条件下的稳定性验证,及与传统静脉采血的一致性对比,充分证实了该方法的可靠性。
通过两项案例研究进一步验证其应用价值:一是Ensure奶昔干预研究,系统揭示了个体对复合膳食的代谢与免疫应答异质性,并构建了涵盖碳水、脂质、氨基酸代谢、胰岛素分泌及炎症反应的六项代谢评分系统,精准量化个体化反应;二是“24/7高频监测”研究,结合可穿戴设备数据,成功捕获了332种分子的昼夜节律特征及饮食、药物的动态体内响应,并通过自主开发的laggedCor算法,揭示了可穿戴数据与体内分子间的潜在因果关联。