
文章标题:Small intracellular vesicles outperform small extracellular vesicles in uptake, drug delivery and retinal neuroprotection
发表期刊:nature biomedical engineering
影响因子:26.6
客户单位:天津医科大学眼科医院
百趣提供服务:经典脂质组学
文章简介
研究团队在nature biomedical engineering期刊发表了题为 “Small intracellular vesicles outperform small extracellular vesicles in uptake, drug delivery and retinal neuroprotection” 的研究。该研究建立了一种从多种细胞类型中简单高效分离小细胞内囊泡(small intracellular vesicles, sIVs)的方法,并系统揭示了其在细胞摄取、药物递送及视网膜神经保护方面,相较于小细胞外囊泡(small extracellular vesicles, sEVs)的显著优势。
研究背景
小细胞外囊泡(sEVs),如外泌体,因其固有的治疗特性及作为生物活性分子天然载体的能力而受到广泛关注。然而,传统sEVs存在产量低、稳定性差、分离流程复杂且耗时久等局限,限制了其临床转化;人工工程囊泡又常伴随生物功能改变或效果降低。值得注意的是,细胞内天然存在大量源自内质网、高尔基体等内膜系统的纳米囊泡(sIVs),参与细胞生理与代谢过程,负责蛋白质、RNA等物质的定向转运,对维持细胞稳态至关重要。但是,这类细胞内囊泡的治疗潜力长期未被探索。
百趣代谢组学
技术路线
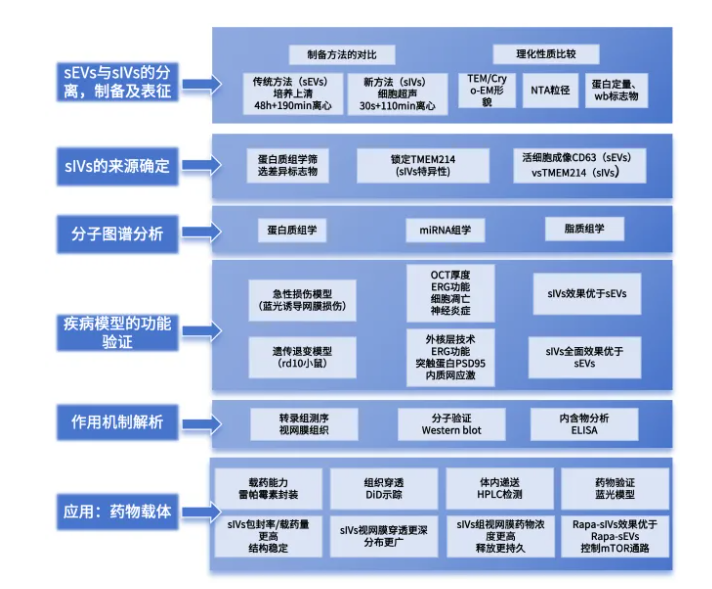
研究结果
01.sIVs的基础优势:体积更小、产量更高、稳定性更强
该研究从细胞内分离并定义了一类新型纳米囊泡——小细胞内囊泡(sIVs),并与当前研究热点小细胞外囊泡(sEVs,如外泌体)进行了系统比较。在制备效率方面,sEVs的分离需经细胞分泌48小时及后续190分钟离心,而sIVs仅需30秒超声破碎结合110分钟离心,总处理时间缩短58%,产量却提高20至40倍(图1a)。
在基本特性方面,透射电镜与粒径分析显示,sIVs同样具备典型的杯状脂质双层结构,但其直径显著小于sEVs(图1b-e);蛋白组成分析表明,sEVs高表达经典外泌体标志物(如CD63、Alix),而sIVs对这些标志物呈低表达或不表达状态,提示二者具有不同的亚细胞起源(图1h-i)。尤为重要的是,在模拟生理条件的37°C环境中孵育24小时后,sEVs大量破裂、数量锐减,而sIVs保持形态完整与数量稳定(图1j-k),这一优越的温度稳定性为其体内应用奠定了基础。
为明确sIVs的生物学起源,该研究先通过蛋白质组学筛选sIVs与sEVs的差异蛋白,锁定TMEM214为sIVs特异性标志物;再利用高分辨率活细胞成像技术,以绿色荧光标记sEVs标志物CD63,红色荧光标记TMEM214。研究发现,CD63标记的大颗粒可穿越细胞膜释放至胞外(即外泌体分泌过程);而TMEM214标记的云雾状小颗粒仅在细胞内部密集穿梭,从未被观察到排出细胞(图1l-m)。
综上,sIVs是细胞内膜系统(如内质网、高尔基体)主动生成的运输载体,构成细胞内物质交流的内在网络,而非细胞破碎后的人工产物。
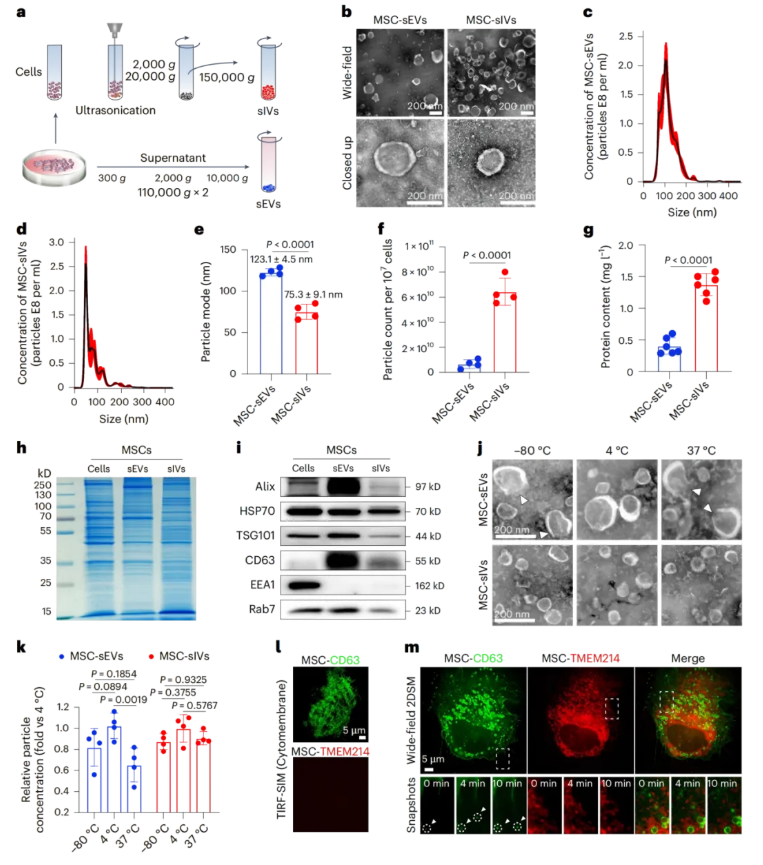
图1.间充质干细胞(MSCs)来源的小细胞外囊泡(sEVs)与小细胞内囊泡(sIVs)的表征
02.sIVs的分子图谱:源自内膜系统的“内部工具包”
在分子层面,sIVs呈现出独特的 “内部工具包” 特征,这与sEVs的分子图谱形成鲜明对比。无标记质谱分析显示,sIVs与sEVs的蛋白分布模式截然不同(图2b),且蛋白含量差异显著(sIVs是sEVs的5-10倍,图1g)。sEVs富含细胞膜蛋白及外泌体标志物,而sIVs则富集内质网、高尔基体相关蛋白及网格蛋白家族——这些正是细胞内负责囊泡运输的核心机器。该研究还对三种细胞来源sIVs共有的106种蛋白进行功能富集分析(图2g-h),发现它们主要参与COPII包被囊泡介导的内质网 - 高尔基体运输、内质网应激调控等细胞内稳态过程。
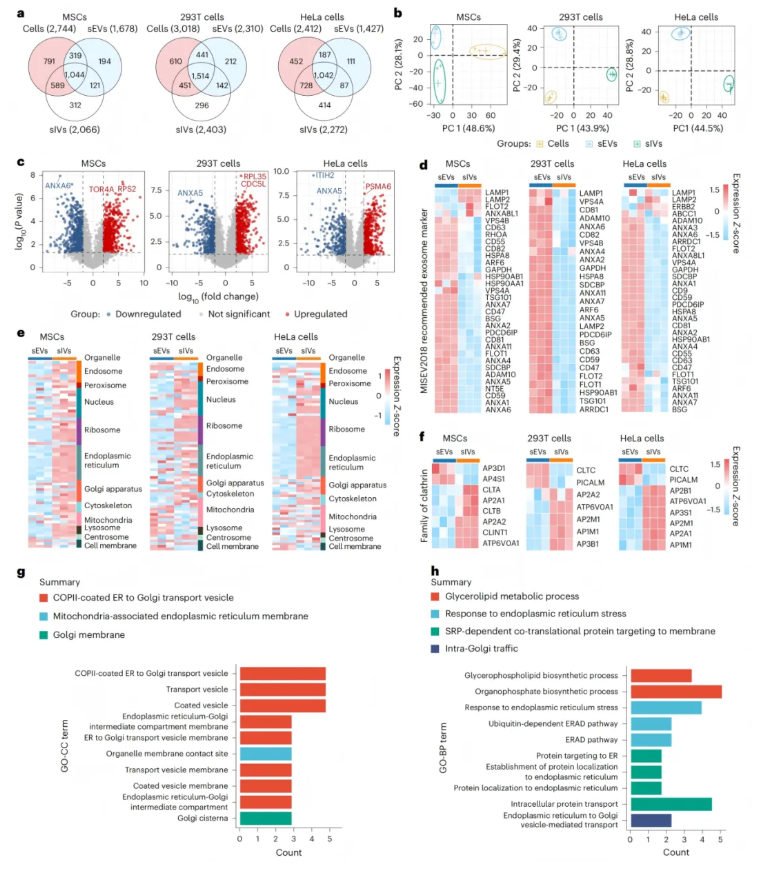
图2.sIVs与sEVs的蛋白质组学分析
之后,研究对三种细胞来源的sEVs与sIVs进行了sRNA测序,重点分析其miRNA谱特征。结果显示,两者sRNA丰度无显著差异(图3a),但sIVs中miRNA占比达90%以上,而sEVs中最丰富的为YRNA(图3b)。MSC细胞来源的sIVs富集的miRNA,其靶基因显著集中于调控细胞内代谢、内质网钙稳态等通路(图3f-g)。不同细胞来源的sIVs所携带的miRNA呈现“细胞类型特异性”,293T细胞来源的sIVs富含调控cAMP通路的miRNA,而HeLa细胞来源的sIVs则携带与神经元突触功能相关的miRNA。
脂质层面,sIVs富含内质网合成的磷脂酰胆碱(PC)、磷脂酰乙醇胺(PE)等甘油磷脂。综上,sIVs的蛋白质、miRNA及脂质构成共同印证了其源自细胞内膜系统的身份,揭示其作为细胞内源性 “工具包” 的多层次调控潜力。
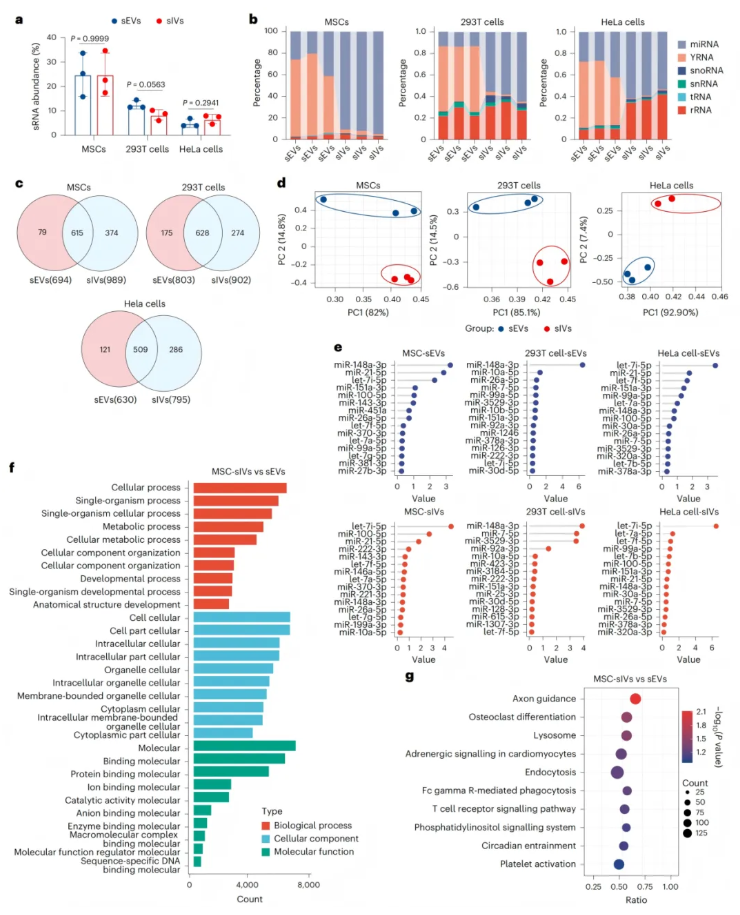
图3.sIVs与sEVs的RNA表达
03.疾病模型验证:急性光损伤视网膜的保护作用
在蓝光诱导的急性视网膜损伤模型中,该研究对MSC来源的sIVs与sEVs开展了系统的比较研究。在结构保护方面,光学相干断层扫描(OCT)、视网膜切片及定量分析结果显示,高剂量sIVs(4 μg)能更有效地维持视网膜厚度,外核层(ONL)感光细胞的存活数量显著高于同等剂量sEVs组;低剂量sIVs(2 μg)与sEVs组无显著差异(图4a-e)。从功能恢复来看,视网膜电图(ERG)检测表明,sIVs能够显著改善感光细胞功能(a波)和双极细胞功能(b波),其效果优于sEVs(图4f-g);同时,高剂量sIVs组中,感光细胞特异性标志物视紫红质的表达水平显著更高,提示其保留效果更优(图4h-i)。
sIVs在抗凋亡与抑制神经胶质增生方面同样表现突出:TUNEL染色证实,sIVs显著减少了外核层凋亡细胞,并在分子水平上下调促凋亡蛋白(Cleaved caspase3、Bax)、上调抗凋亡蛋白(BCL-2);此外,sIVs还能更有效地抑制Müller细胞(GFAP标志物)和小胶质细胞(IBA1标志物)的异常活化,从而减轻视网膜神经炎症相关反应(图4j-k)。综上,在急性光损伤模型中,高剂量sIVs在结构保护、功能恢复及抗凋亡、抑制神经胶质增生等方面均展现出优于sEVs的治疗潜力。
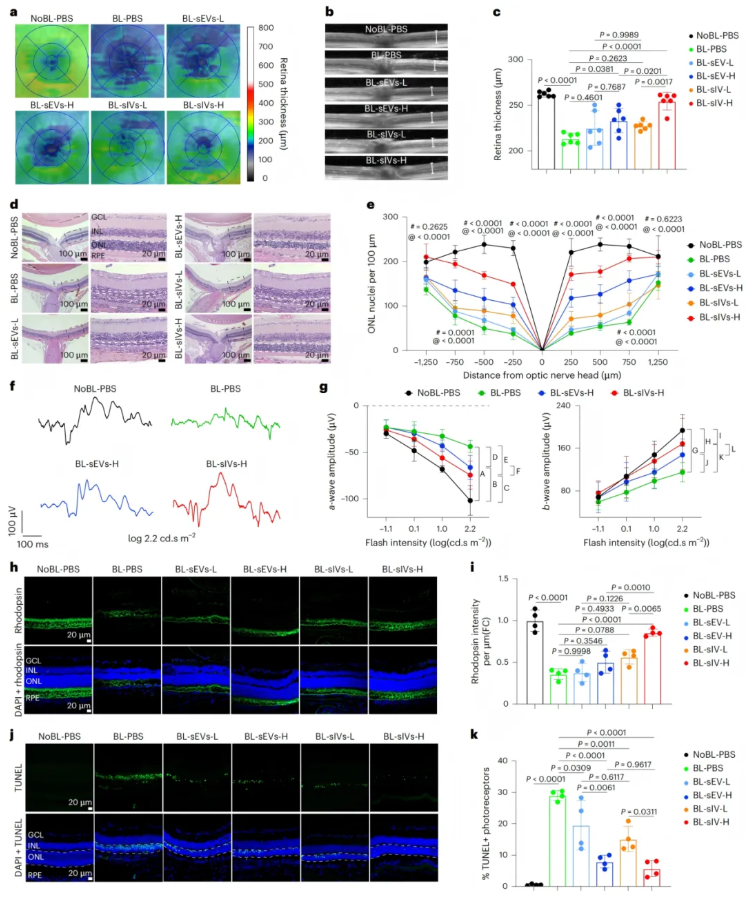
图4.MSC-sIVs与MSC-sEVs对蓝光损伤小鼠的治疗效果
04.疾病模型验证:遗传性视网膜退行性变(rd1小鼠)的治疗效果
在rd10小鼠模型(因Pde6b基因突变模拟人类视网膜色素变性的慢性进行性疾病)中,sIVs的治疗效果显著优于sEVs。实验中于rd10小鼠出生后13天(p13)进行玻璃体内注射治疗,出生后28天(p28)评估疗效。结构上,p28的rd10小鼠感光细胞层已大量丢失,而sIVs治疗显著保留了外核层(ONL)的细胞核数量,效果明显优于sEVs(图5a-b);同时,sIVs对感光细胞特异性标志物视紫红质的表达保留效果显著优于sEVs,进一步证实其对感光细胞的保护作用(图5e-f)。
功能上,rd10小鼠的视网膜电图波形近乎消失,sIVs在所有刺激强度下均能显著恢复a波和b波振幅,且在最高刺激强度下的a波、中高刺激强度下的b波恢复效果优于sEVs;而sEVs仅在中高刺激强度表现出部分改善(图5c-d)。此外,sIVs还展现出更强的突触保护作用:感光细胞突触连接关键蛋白PSD95的表达在sIVs治疗后得到显著挽救(图5g-h)。
机制上,sIVs显著减少了外核层凋亡细胞,并有效调节凋亡相关蛋白(下调Cleaved-caspase3、Bax,上调BCL-2),而sEVs几乎无效(图5i-j);同时,sIVs能更有效地抑制rd10小鼠视网膜中Müller细胞和小胶质细胞的异常活化,减轻神经胶质增生相关炎症反应。
综上,sIVs在遗传性视网膜退行性病变的治疗中,对于结构保护、功能恢复、突触维持、抗凋亡及抗炎等多方面展现出综合优势。
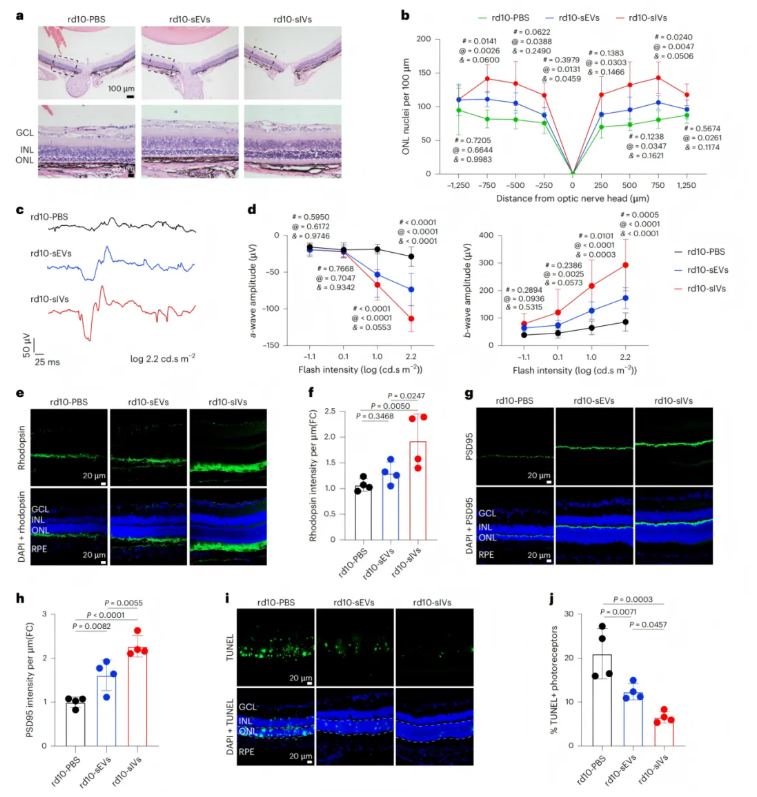
图5.MSC-sIVs与MSC-sEVs在rd10小鼠模型中的治疗效果
05.机制解析:sIVs的作用途径
该研究明确了sIVs发挥视网膜神经保护作用的两大核心途径,也是其疗效优于sEVs的关键所在。已知内质网(ER)应激是蓝光损伤和遗传性视网膜退行性变的核心病理环节,持续激活会诱发视网膜细胞凋亡,而sIVs可通过自身分子组成精准靶向调控该通路:RNA测序显示,sIVs治疗能显著下调蓝光损伤、rd10小鼠视网膜中的ER应激相关通路表达(图6a-b);其蛋白谱富集 “负调控内质网应激” 相关功能,携带的前50个高丰度差异miRNA还可靶向调控 “内质网钙稳态” 通路,双重作用抑制ER应激(图6c-d)。
Western blot验证证实,sIVs能显著降低两种模型中GRP78、CHOP等ER应激标志物的异常升高,蓝光损伤模型中sEVs无明显作用,rd10模型中sEVs的抑制效果也远弱于sIVs(图6e-g)。此外,sIVs还富集bFGF、IGF-1等神经营养因子及抗炎因子,可营造视网膜保护性微环境,与ER应激抑制作用协同增效。
综上,sIVs通过精准靶向缓解内质网应激+富集营养因子构建保护微环境的双重机制,实现了优于sEVs的多重视网膜神经保护效果。

图6.MSC-sIVs对光损伤小鼠及rd10小鼠视网膜内质网应激的抑制作用
06.应用拓展:sIVs作为“超级药物载体”
为评估sIVs的药物递送潜力,该研究以难溶性药物雷帕霉素为模型,从载药能力、体内递送及协同疗效展开系统验证(图7a)。sIVs展现出先天载药优势,对雷帕霉素的包封率、载药量均显著高于sEVs,体外药物累积释放量也更优(图7b-c)。经结膜下、玻璃体内两种途径注射后,载药sIVs在视网膜中的药物浓度显著高于载药sEVs组和游离药物组,游离药物因溶解度低、易结晶,疗效微弱(图7d-e)。在蓝光损伤模型中,等效雷帕霉素剂量下,载药sIVs在挽救视网膜厚度、改善电生理功能、抑制细胞凋亡,以及阻断mTOR通路激活方面,疗效均显著优于载药sEVs,而空囊泡组无明显治疗效果(图7f-k)。综上,sIVs凭借高载药能力、强组织穿透性,结合自身固有神经保护活性,成为兼具 “药物载体” 与 “治疗剂” 双重功能的眼底疾病治疗创新平台。
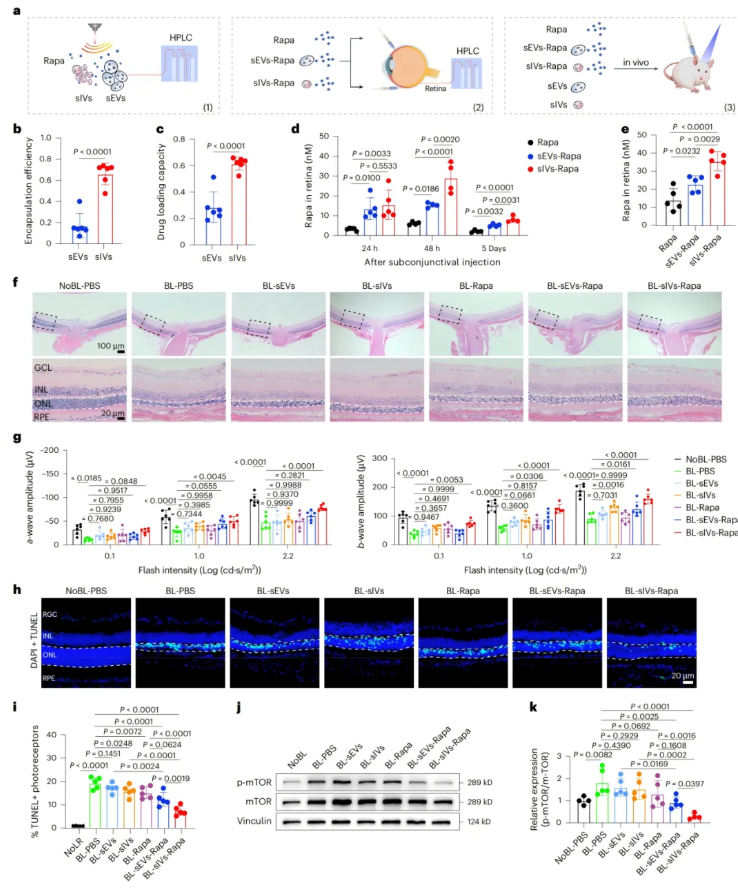
图7.雷帕霉素(Rapa)负载的sEVs与sIVs在蓝光损伤小鼠中的载药能力及治疗效果比较
研究总结
该研究揭示小细胞内囊泡(sIVs)的治疗潜力。相较热门的小细胞外囊泡(sEVs),sIVs粒径更小,制备效率显著更高,生理温度下稳定性更强,组织穿透力更优,且以TMEM214为特异性标志物。sIVs源自内膜系统,富含内质网/高尔基体蛋白、磷脂酰胆碱(PC)与磷脂酰乙醇胺(PE)及调控性miRNA,构成独特的 “内部工具包”。sIVs通过靶向抑制内质网应激、富集神经营养因子及抑制神经胶质增生,在急性和遗传性视网膜退行性疾病模型中均实现优于sEVs的结构与功能保护。sIVs对亲脂性药物的载药与递送效率更优,兼具协同增效作用。sIVs凭借独特的功能,为纳米药物递送体系研发以及视网膜神经保护治疗,提供了全新的思路与可行方案。