
英文标题:Spatial metabolomics revealed mTOR-mediated gastric epithelial repair by licorice (G. inflata) flavonoids
中文标题:空间代谢组学揭示胀果甘草黄酮通过mTOR介导调控胃上皮修复
发表期刊:Food Research International
影响因子:8.0
研究背景
过量饮酒是诱发胃溃疡的重要危险因素,高浓度酒精会破坏胃黏膜屏障,引发氧化应激与炎症浸润,抑制上皮修复。胃黏膜修复是高度依赖ATP的能量代谢过程,糖酵解、三羧酸循环及线粒体功能紊乱会阻碍损伤愈合。
甘草(Glycyrrhiza inflata)作为我国经典药食同源中药材,其活性组分甘草黄酮(Licorice flavonoid, LF)已被证实具有抗炎、抗氧化及胃黏膜保护作用。现有研究表明,LF可通过PI3K/AKT通路抑制细胞凋亡、经EGFR/ERK通路促进黏膜再生,对酒精性胃溃疡具有显著改善效果。但LF生物利用度较低,其在胃组织局部如何调控代谢网络、驱动黏膜修复的分子机制尚未系统阐明。
mTOR通路作为细胞能量感应与代谢调控核心节点,可感知营养与能量状态,调控细胞增殖、迁移及能量代谢,在胃黏膜损伤修复中发挥关键作用。鉴于传统代谢组学难以揭示组织层面代谢物空间分布特征,本研究整合非靶标代谢组学与MALDI-MSI空间代谢组学技术,用以探究LF改善酒精性胃黏膜损伤的代谢调控机制。
技术路线
研究结论
01.胃溃疡大鼠中LF的药代动力学特征
首先,研究建立了可同步定量大鼠血浆中5种LF活性成分(LCB、LG、ILG、LFA、LCA)的高灵敏度LC-MS/MS检测方法。经验证,此方法空白血浆对目标分析物无显著基质干扰(图1A-C),各项指标及结果正常稳定。基于该方法,5种成分的血浆浓度-时间变化曲线(图1D-H)被绘制,经DAS软件计算获得胃溃疡大鼠的主要药代动力学参数(表1)。结果表明,LF口服后吸收迅速,5种成分达峰时间(Tmax)为0.395~1.445h,其中LG吸收最快,LCA吸收最慢;成分消除半衰期(T1/2z)为7.688~16.215h,表明LF在体内消除缓慢,具备长效作用潜力。其中,LCA的Cmax、AUC均最高,为最主要吸收入血成分,其余4种成分口服生物利用度相对较低。此外,胃组织检测证实,LCA、LG、ILG可在胃组织稳定检出,表明其兼具血液吸收与胃黏膜亲和性,可通过胃部局部滞留直接发挥抗溃疡活性。简言之,LF经口服后可快速到达胃黏膜,消除缓慢,其中LCA是血浆中主要的暴露成分,而多种成分通过黏膜亲和性实现局部滞留,有利于后续的胃黏膜保护及修复。
图1.LCB、LG、ILG、LFA、LCA的提取总离子流图与血浆浓度—时间曲线
表1.胃溃疡模型大鼠灌胃给予LF后5种成分的药代动力学参数
02.LF对胃溃疡大鼠胃黏膜损伤及胃酸分泌的改善作用
通过肉眼观察和组织病理学评估,研究明确了LF对酒精诱导的胃溃疡大鼠胃黏膜损伤的改善作用,结果如下:
①宏观形态学观察显示,酒精灌胃可造成大鼠胃黏膜结构破损、表面粗糙,伴点状/线状出血、多发糜烂溃疡及水肿;但经LF干预后,大鼠胃溃疡指数显著降低,仅见散在的点状糜烂和少量出血(图2A-B),其中低、高剂量LF组的溃疡抑制率分别达52.8%、77.8%,量效关系明确。
②组织病理学检测证实,LF与阳性对照药奥美拉唑(OME)均可显著减轻胃组织出血性病变、黏膜溃疡、炎症浸润与水肿,同时促进胃上皮修复,维持胃腺体结构完整(图2C-D)。
③分子水平检测发现,酒精可显著上调胃酸分泌关键效应分子ATP4α、CCKBR的mRNA表达,诱导胃酸过度分泌;而LF可显著逆转该异常变化,表明LF可通过调控上述靶基因表达,抑制病理性胃酸分泌,发挥胃黏膜保护作用(图2E-F)。综合而言,LF显著减轻了酒精引起的胃黏膜损伤,促进上皮修复,并抑制胃酸分泌,表现出良好的抗胃溃疡作用。
图2.LF干预对胃溃疡的改善、氧化应激的抑制及炎症浸润的缓解作用
03.LF减轻胃溃疡大鼠的氧化应激与炎症浸润
氧化应激与炎症反应是酒精性胃黏膜损伤的核心病理机制。抗氧化酶作为机体第一道防线,对维持抗氧化能力至关重要。经检测,酒精暴露可显著下调大鼠胃组织中CAT、GSR、GPX、NQO1、SOD1、SOD2共6种关键抗氧化酶的表达,破坏机体抗氧化防御体系;而LF干预可显著逆转上述酶活性的下降,增强胃黏膜抗氧化能力,促进溃疡修复(图2G-L)。在炎症浸润方面,酒精可诱导胃黏膜及黏膜下层大量巨噬细胞浸润,LF(尤其高剂量组)可显著抑制该效应(图2M-N);同时,LF还逆转了酒精诱导的炎症趋化因子MCP-1(黏膜下层)与黏附分子ICAM-1(黏膜)的表达上调(图2M-P),进一步减轻炎症细胞的募集与浸润。因此,LF可通过增强胃黏膜抗氧化能力、抑制炎症细胞浸润,发挥胃黏膜保护作用。
04.LF改善酒精诱导的代谢紊乱
为探究LF对胃溃疡(GU)大鼠体内代谢物的调控作用,研究进一步采用UPLC-Orbitrap-MS进行代谢组学分析。总离子流图显示,各组代谢物轮廓存在显著差异(图3A),LF治疗调节了酒精导致的代谢物紊乱。主成分分析显示,质控样本(QC)聚集良好(图3B-C),表明数据稳定性高;同时,LF高剂量组与正常对照组(NC)更接近,而与GU组显著分离,初步说明LF可改善代谢扰动。OPLS-DA进一步验证了组间代谢差异:GU组与NC组(图3D,F)、LF高剂量组与GU组(图3H,J)的代谢谱均明显区分;200次置换检验结果证实所有模型均无过拟合问题(图3E,G,I,K),数据分析结果可靠,能够准确反映LF对胃溃疡大鼠代谢的调控效应。综上,代谢组学数据揭示了LF通过调节代谢紊乱发挥治疗作用;同时,LF可能通过多靶点代谢调控改善酒精诱导的胃黏膜损伤,具有潜在的临床应用价值。
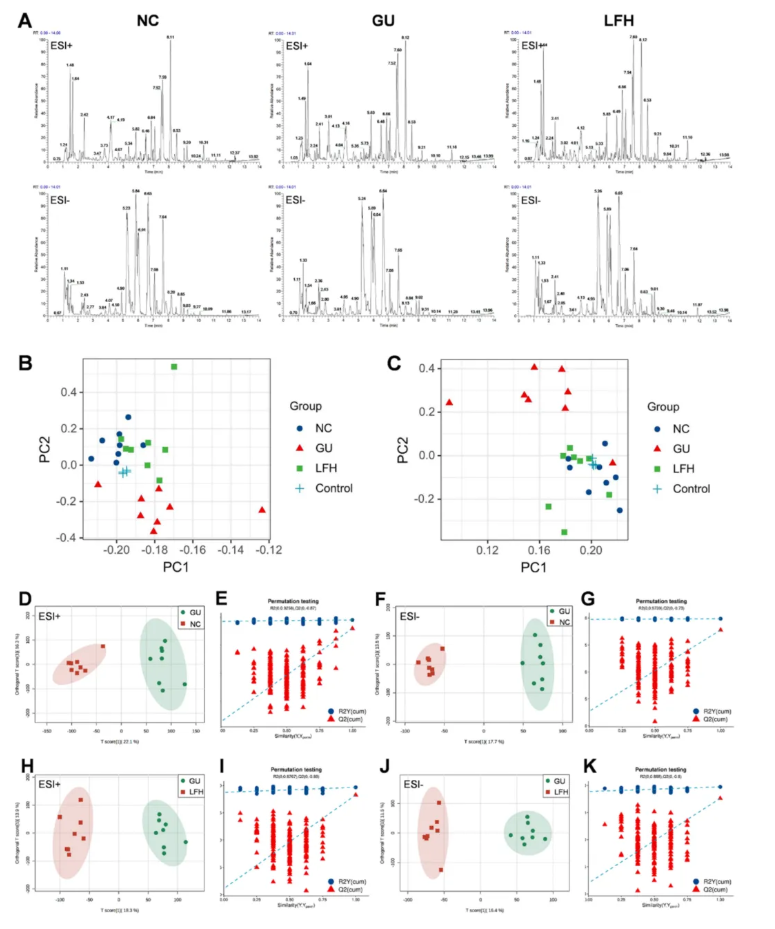
图3.基于尿液样本的代谢组学多元统计分析
05.LF干预下的代谢通路与生物标志物分析
根据不同VIP值与p值标准,总计81个显著差异代谢物(SDEMs)在正常组(NC)、胃溃疡组(GU)和高剂量甘草黄酮组(LFH)中被鉴定,其中正离子模式36个、负离子模式45个。在NC与GU组差异代谢物(DEMs)的通路富集中,共计15条核心通路影响值>0.1,其中包括核黄素代谢、谷胱甘肽代谢、苯丙氨酸代谢、维生素B6代谢等(图4A)。与GU组相比,LFH组共有33个DEMs可被LF成功逆转(图4B)。具体而言,LF可上调核黄素、生物素、苯乙胺、苯乙酰甘氨酸、吡哆醇及辅酶A的水平,下调吡哆胺含量。这些代谢物主要参与糖酵解、三羧酸循环等能量代谢过程,为黏膜修复提供能量支持。为进一步明确其在胃黏膜不同分层的原位作用机制,本研究后续开展了MALDI-MSI分析。
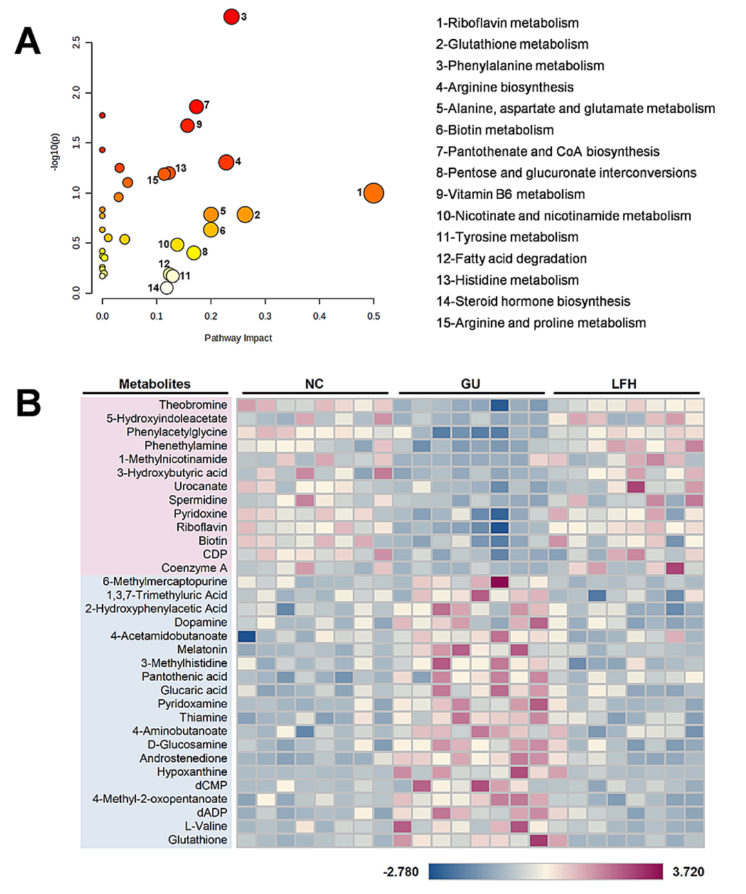
图4.代谢通路与生物标志物多元统计分析
06.基于MALDI-MSI验证胃溃疡代谢标志物及LF的调控作用
06.1-代谢差异主要存在于胃壁各层,而非全胃组织
在MALDI-MSI技术的加持下,研究首先对全胃组织切片进行了差异代谢物分析。依据前期预设筛选条件,通过将胃壁划分为黏膜层(M)、黏膜下层(SM)和肌层(MC)后,组间代谢差异得以显现(图5A-C)。结果而言,黏膜层是胃溃疡发生与修复的核心部位。正常组(NC)与溃疡组(GU)在该层的代谢物差异最为显著(图5A)。当溃疡发生时,辅酶A、花生四烯酸、AMP、ADP等关键代谢物水平显著降低。进一步对黏膜层进行KEGG富集分析(图5D、E),可以明确,酒精诱导的胃溃疡可显著干扰PI3K-Akt、mTOR、FoxO等信号通路;且经LFH干预后,差异代谢物亦同样富集于上述通路,与该团队前期研究结果一致。
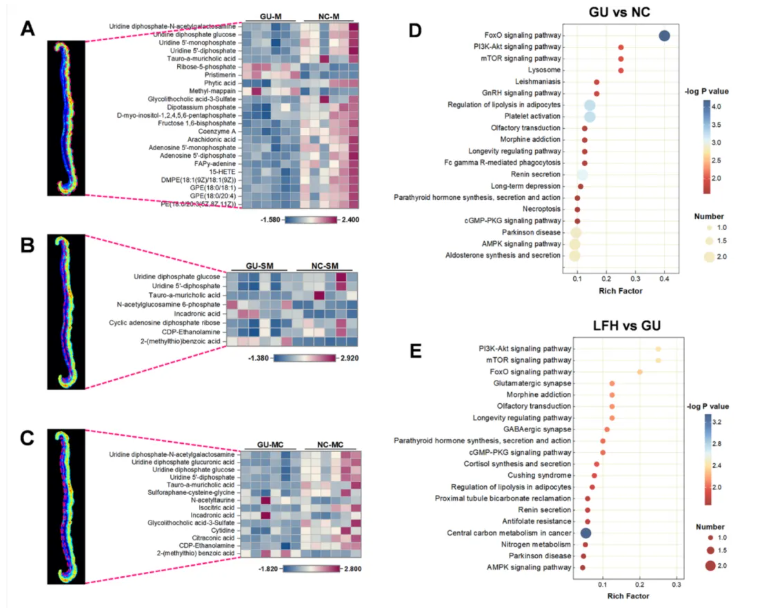
图5.胃不同组织层SDEMs及KEGG富集分析
06.2-胃溃疡所致核酸代谢紊乱及LF的修复作用
胃肠道黏膜损伤后的快速上皮再生是高度依赖ATP的能量代谢过程。通过MALDI-MSI技术,研究发现,与核酸代谢相关的ATP、GDP、GTP、AMP、ADP等多种代谢物在胃溃疡大鼠胃壁不同层次中发生了显著变化。具体而言,在胃黏膜层中,胃溃疡组(GU)核酸代谢物水平较正常组显著降低;但经LF干预后,ATP、GTP、GDP水平显著回升,ADP、AMP亦呈轻度上调趋势(图6A–E)。此外,肌层中GTP变化趋势与黏膜层基本一致;而黏膜下层中ADP、AMP、GDP在LF干预后未见明显改变。简单来说,LF可特异性上调胃黏膜层核酸代谢相关物质水平,提升了ATP合成能力,为黏膜修复提供充足能量供给。
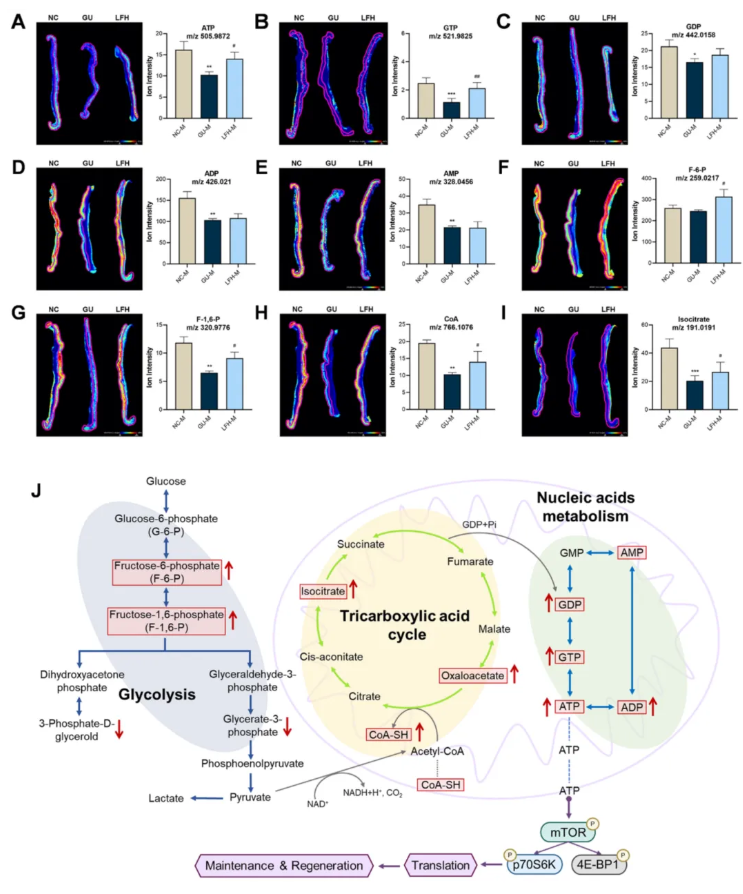
图6.基于MALDI-MSI的胃溃疡能量代谢紊乱及LF的干预作用
06.3-胃溃疡引发糖酵解与TCA循环紊乱及LF的调控作用
胃肠道黏膜正常生理功能与损伤修复的能量供应,主要依赖糖酵解与TCA循环通路协同维持。经MALDI-MSI检测,在胃黏膜内仅果糖-6-磷酸(F-6-P)和果糖-1,6-二磷酸(F-1,6-P)显示出明显的质谱信号(图6F-G)。与GU组相比,LFH组黏膜层中的F-6-P和F-1,6-P含量均显著升高;其中F-1,6-P在肌层中也出现升高。在TCA循环体系中,辅酶A、异柠檬酸、苹果酸及草酰乙酸等核心代谢物被检测。酒精损伤可显著降低胃黏膜层辅酶A表达,而LF可有效逆转该异常,并改善黏膜下层与肌层的辅酶A代谢失衡(图6H)。同时,LFH处理显著提升了黏膜层与肌层异柠檬酸水平(图6I)。由此可见,酒精可在胃黏膜层、黏膜下层及肌层多部位诱发糖酵解与TCA循环紊乱,且病变以黏膜层最为显著。LF可通过靶向调控能量代谢关键代谢物,有效修复胃组织能量代谢障碍,进而改善胃黏膜损伤(图6J)。
07.LF调控胃黏膜能量代谢与线粒体动态以促进损伤修复
糖酵解、三羧酸循环及线粒体功能是胃肠道能量供应的核心环节。在胃溃疡模型组中,葡萄糖与ATP含量显著降低,能量合成受阻(图7A-B);而经不同剂量LF干预后,二者水平均显著回升。同样地,胃黏膜损伤也下调了葡萄糖转运蛋白GLUT1表达,但亦会被LF所逆转,细胞对葡萄糖的摄取能力得以加强(图7C、H)。在能量代谢关键酶方面,LF显著提高了糖酵解通路及TCA循环相关基因表达,有效逆转酒精所致的酶活性抑制,全面激活能量代谢通路(图7F-G)。线粒体稳态检测显示,LF干预可恢复线粒体外膜标志蛋白TOMM20表达,回调线粒体质量控制及动力学相关基因水平,改善线粒体结构与功能异常(图7C、H、I)。综上所述,LF可通过提升葡萄糖摄入、促进ATP生成、激活糖酵解与三羧酸循环、修复线粒体稳态,为胃黏膜修复再生提供充足能量,从而发挥抗胃溃疡作用。
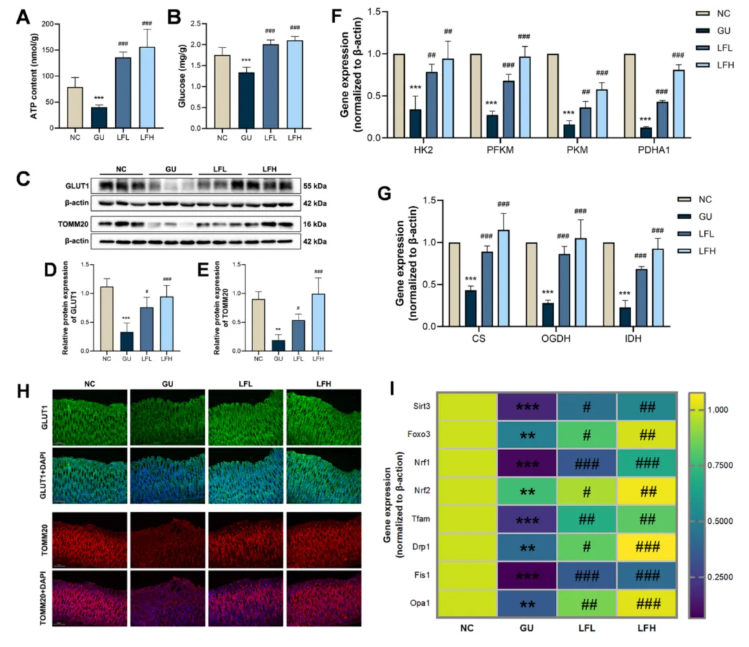
图7.LF对能量代谢相关分子及线粒体动力学的促进作用
08.LF通过激活mTOR与糖酵解通路促进胃黏膜修复再生
EGF、TGF-α、HGF、IGH等生长因子是调控胃黏膜上皮增殖、迁移与再上皮化的关键分子,可通过激活mTOR通路介导代谢、运动与细胞增殖。与正常组相比,胃溃疡组的相关生长因子表达显著下调,而低、高剂量LF均可显著上调其表达(图8A-D)。类似地,模型组p-mTOR、p-p70S6K、p-4EBP1、Hif-1α表达也显著受抑,但可被LF所激活(图8E-I)。此外,胃溃疡组胃黏膜(尤其黏膜表层)p-mTOR与HK2表达显著降低;LF干预后二者表达同步明显回升(图8J);同时,LF显著上调糖酵解关键限速酶HK2、PFKM、PKM2、LDHA的表达(图8K-O)。整体而言,LF可通过上调生长因子表达,协同激活mTOR信号通路与下游糖酵解通路,强化能量代谢供给,进而促进胃黏膜损伤修复与再生。
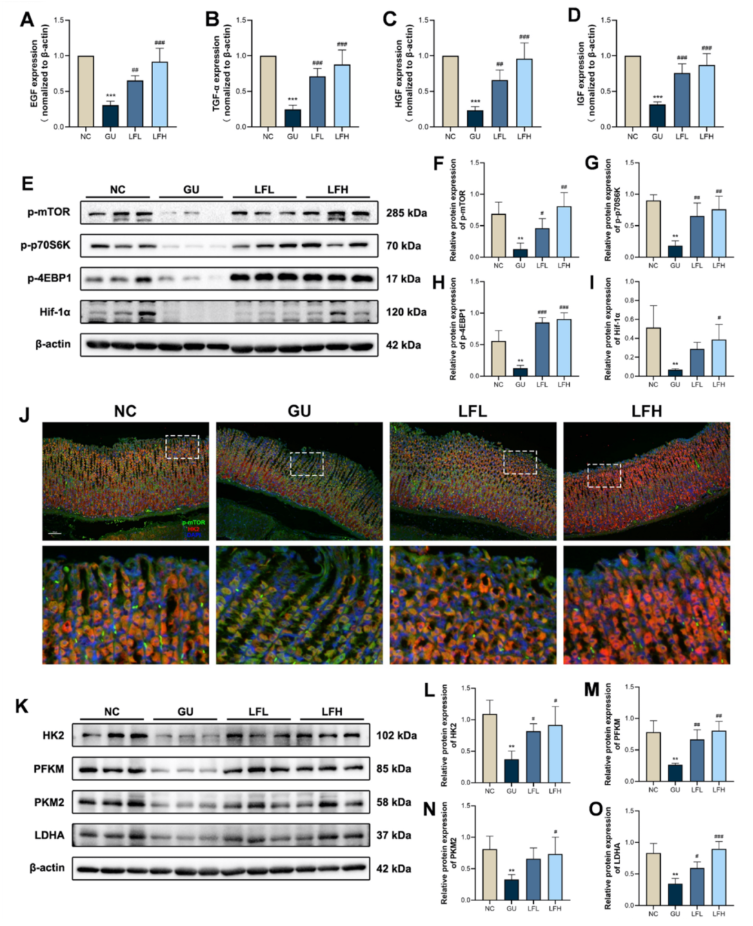
图8.LF通过激活mTOR与糖酵解通路发挥胃黏膜修复及再生作用
09.维生素B族代谢物提升ATP水平并激活mTOR信号通路
基于前期血清与尿液代谢组学结果,可以明确,LF干预可共同富集7条代谢通路,其中烟酸与烟酰胺(维生素B3)代谢通路差异显著(图9A)。与胃溃疡模型组相比,LF可显著上调该通路关键代谢物烟酰胺、1-甲基烟酰胺的表达(图9B)。以人胃黏膜GES-1细胞开展体外验证,酒精刺激会造成细胞损伤,降低ATP水平,并抑制mTOR通路关键蛋白p-mTOR、p-p70S6K及p-4EBP1的活化。而维生素B3预处理则能有效逆转上述异常,缓解能量代谢障碍,明显恢复mTOR通路活性(图9D-G)。综上,维生素B3是LF调控的重要功能性代谢物质,能够提升细胞ATP合成、激活mTOR信号,与LF作用模式一致。
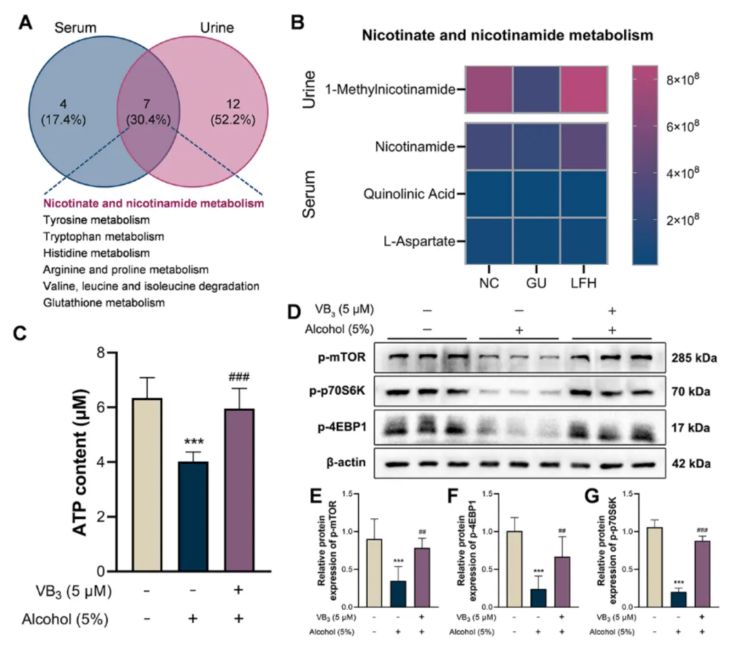
图9.B族维生素相关代谢物可提高ATP含量并激活mTOR通路
研究总结
本研究采用非靶标代谢组学与空间代谢组学(MALDI-MSI)联合策略,系统阐释甘草黄酮(LF)改善酒精性胃溃疡的分子机制。结果表明,LF口服吸收快、消除慢,可通过胃黏膜亲和性局部富集;能显著减轻胃黏膜损伤、抑制胃酸过度分泌、增强抗氧化酶活性并缓解炎症浸润。代谢组学证实LF可逆转酒精所致B族维生素、糖酵解、TCA循环及核酸代谢紊乱;结合空间代谢组,进一步证实LF主要在胃黏膜层修复能量代谢障碍,提升ATP生成。机制上,LF通过上调EGF、TGF-α等生长因子激活mTOR通路,促进糖酵解关键酶表达,并改善线粒体生物发生与动力学平衡;体外验证明确维生素B3可模拟LF作用,提升ATP水平并激活mTOR。综上,LF通过调控“能量代谢—激活mTOR—修复胃黏膜上皮”的级联效应发挥抗溃疡作用,为其功能产品开发提供科学依据。